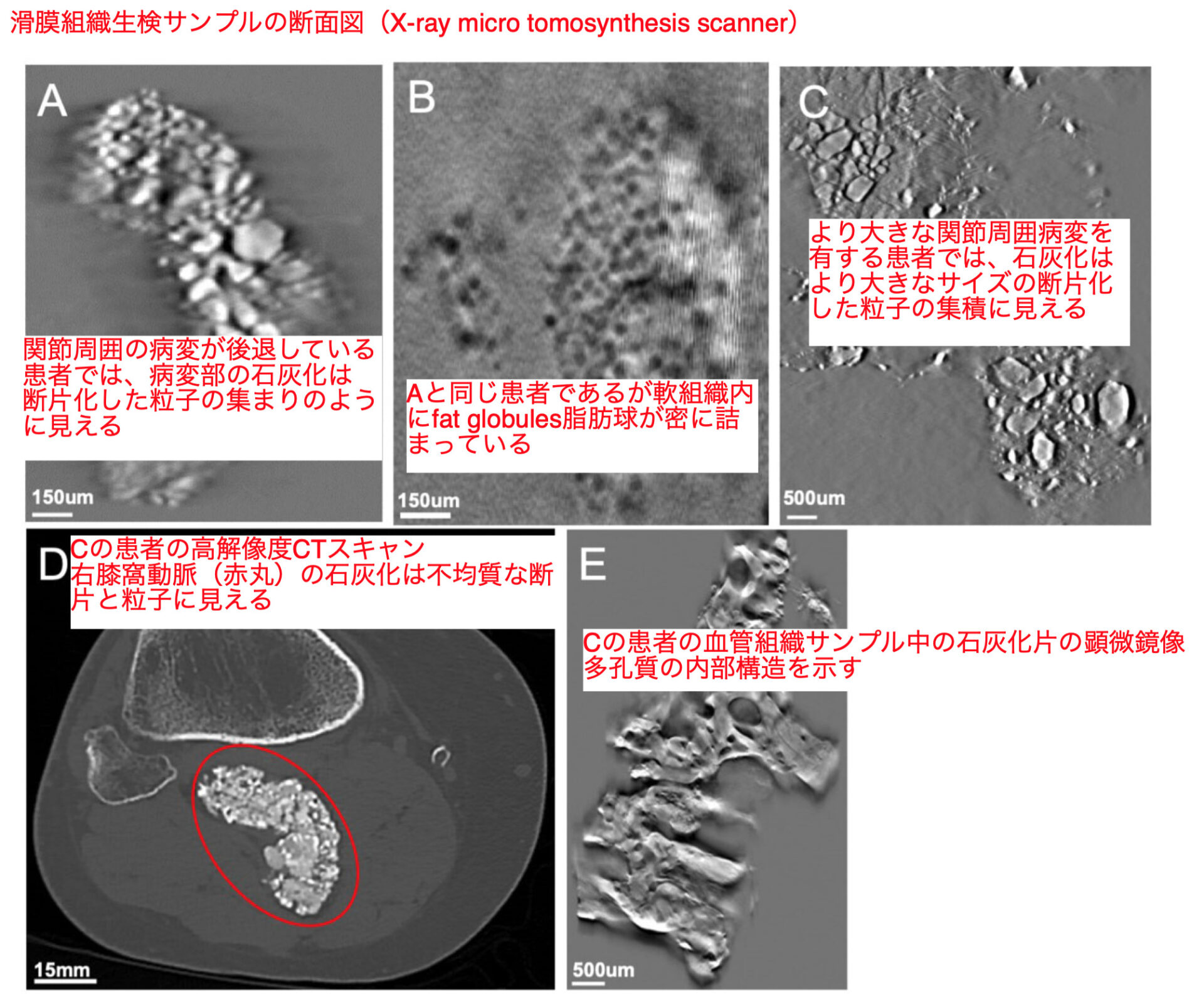
Multifocal calcific periarthritis with distinctive clinical and radiological features in patients with CD73 deficiency.
Rheumatology (Oxford). 2021 Dec 24;61(1):163-173.
Rheumatology key messages
-
Arterial calcification due to deficiency of CD73 (ACDC) は常染色体劣性遺伝性の疾患であり、CD73をコードするNT5E遺伝子の変異によって引き起こされる
-
ACDC患者は、炎症性関節炎に加えて重度の動脈石灰化を発症する
-
ACDC患者の滑液と関節周囲の石灰化には、ハイドロキシアパタイト結晶が認められた
【背景】
-
ACDCは、CD73欠損による動脈石灰化症は CD73をコードしている ecto-5′-nucleotidase (NT5E) geneのLoss of funcation変異によって起こる hereditary遺伝性の hautosomal recessive ectopic mineralization syndrome常染色体劣性異所性石灰化症候群である N Engl J Med 2011; 364:432–42.
-
CD73は、5′-リボヌクレオチドホスホヒドラーゼ酵素活性を持つグリコシルホスファチジルイノシトールアンカー糖タンパク質であり、細胞外のアデノシン一リン酸(AMP)をアデノシンと無機リン酸(Pi)に変換する Arterioscler Thromb Vasc Biol 2019;39:339–48.
-
CD73の欠損は、細胞外アデノシンの減少や組織の非特異的アルカリホスファターゼ活性の増強と、それに伴う無機ピロリン酸(PPi)の加水分解の増加、PPi/Pi比の減少を通じて、間接的に組織の石灰化を促進すると考えられている Sci Signal 2016;9:ra121.
-
PPiは強力なanti-mineralization factorであり、その濃度が減少すると自発的な軟骨形成と動脈石灰化が促進される Proc Natl Acad Sci USA 2002;99:9445–9.
-
軟組織および血管の石灰化の臨床症状は、慢性腎臓病、動脈硬化、糖尿病、慢性的なワルファリン使用および高齢でも観察される Vascul Pharmacol 2016;84:8–14.
-
ACDCでは、早期に発症した動脈石灰化は主に下肢を障害し、症候性の跛行を引き起こす N Engl J Med 2011; 364:432–42.
-
また、手・手首・足首・足の関節包周囲の石灰化も、報告されている Int J Cardiol 2016;212:248–50.
ACDCに伴う関節炎の臨床的特徴については、これまで体系的に検討されてこなかった
この論文の目的は遺伝的に定義された疾患を持つACDC患者8名の関節病変の臨床的、放射線的、病理学的所見について報告すること
-
結果として、ACDCは、X線画像診断により関節包と関節周囲の両方に、浸食性の関節腔狭小化と多発性石灰化を示す変化に加えて、小関節に時折起こる炎症症状を示す特徴的な病態を示すことが明らかとなった
-
関節炎はしばしば機能制限を伴う固定変形を引き起こすこともわかった
-
関節の病変は、ほとんどの患者で血管の症状に先行しするため、最初にリウマチ専門医を受診することが多いACDCの臨床的・放射線学的な特徴は他の関節炎とは異なり、疑った場合には潜在性の血管病変の可能性やNT5E遺伝子検査を施行し、調査する必要がある
【方法】
-
遺伝学的にACDC病と確認された8名の患者を対象にリウマチ様症状および関節病変のパターンを評価した
-
すべての患者は米国国立心肺血液研究所(NHLBI)のいくつかのプロトコルに登録されている患者である
-
プロトコルはNHLBIの施設審査委員会で審査・承認され、被験者全員が参加前に文書によるインフォームドコンセントを得ている JAMA 2013;310: 2191–4.
-
遺伝子検査に基づき、すべての患者はNT5E遺伝子にホモ接合性のナンセンス変異または複合ヘテロ接合性の変異がある
-
このコホートでは、念入りな病歴聴取と身体検査、および年1回のリウマチ学的評価を施行した
-
検査評価は複数回の受診時に施行しており、血液検査およびX線検査も施行している。CTとMRIを施行した患者もいる
-
さらに、4名の患者で局所麻酔下で整形外科医による観血的関節生検を実施し、症状のあるMCP関節の滑液、滑膜組織、関節周囲石灰化サンプルを採取した
-
生検後すぐにホルムアルデヒドで固定、パラフィンに包埋、凍結処理され、病理組織学的分析は、ヘマトキシリン・エオジンおよびVon Kossa試薬で染色されたパラフィン包埋切片を用いて行った
-
採取した滑液(30~50μl)は、偏光顕微鏡で分析し、2人リウマチ専門医が検討
-
HE染色とアリザリンレッド染色は、すべての滑液のサンプルで行われた Arthritis Rheum 1983;26: 191–200.
-
石灰化を含む組織は、X-ray diffraction(X線回折)とX-ray microtomosynthesis(X線マイクロトモシンセシス)により、そのmorphology形態とchemical composition化学組成を研究した
-
2名の患者において、periarticular joint calcification関節周囲の石灰化は、以前に大腿骨内膜切除術の際に採取された石灰化した血管とも比較された
【結果】
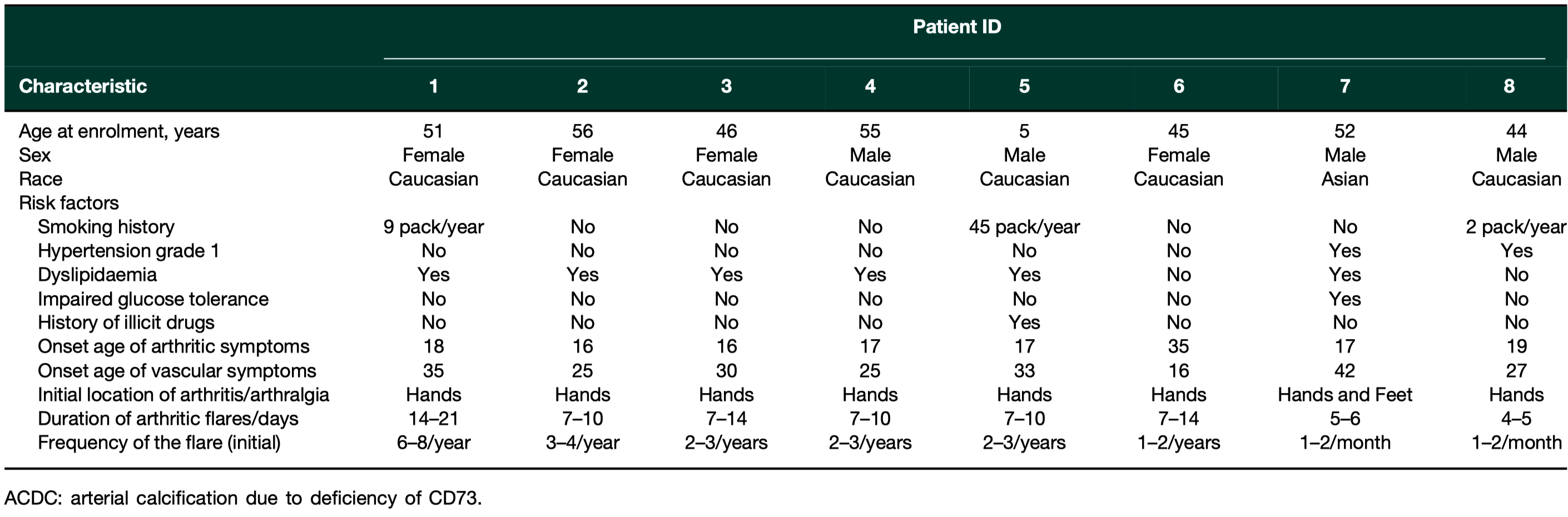
人口統計とリスクファクター
-
NT5E欠損症が遺伝的に確認された4家系8名(1家系5名兄弟)の患者をNIH臨床センターで評価し、3年間〜11年間毎年追跡調査した
-
表1に示すように、関節炎発症年齢の中央値は17歳、vascular phenotype血管型は28.5歳であり、7名/8名中の患者において関節炎症状は血管症状より8-25年先行していた
動脈硬化のリスク因子の患者内訳
-
喫煙歴: 3名
-
違法薬物使用歴: 1 名
-
Mild mixed dyslipidaemia軽度混合型脂質異常症: 6名
-
impaired glucose tolerance耐糖能異常HbA1C 6.3: 1名
-
Grade 1 hypertension: 2名(低用量CCBおよびβblockrにより管理中)
-
副甲状腺機能亢進症・collagen vascular disease膠原病性血管障害・ヘモクロマトーシス・痛風はいずれも認めない
遺伝学的所見
-
ACDCの原因となるNT5E遺伝子の変異は、2011年に9名で認められ、うち6名が本研究の対象となった
-
2名の患者については、臨床症状に基づいてNT5Eスクリーニングが行われた
-
1名ではイントロン3の新規ホモ接合型スプライスサイト変異が同定された[10]
-
1名では既報の変異が見つかった J Hum Genet 2015;60:561–4.
-
-
5 名は変異 c.662C>A (p.S221X) のhomozygousホモ接合体
-
1 名は c.1387C>T (p.R463X) のhomozygousホモ接合体
-
1 名は c.751+2T>C((exon 3 skipping))
-
1名はNT5E遺伝子(NM_002526.3)においてc.662C>Aとc.1609dupA(p.S221X、p.V537fsX7)の複合ヘテロ接合体
リウマチ学的症状および放射線学的データ
-
ACDCが遺伝子的に確認される以前は、すべての患者は臨床評価に基づいてseronegative RA、JIAまたはcrystal-induced arthropathy結晶誘発性関節症と診断されたが、滑液で結晶が確認された患者はいない
-
DIP、PIP、MCP、MTP関節に最長2週間継続する回帰性関節炎は、すべての患者で報告されている
-
概して、これらの関節炎はNSAIDsまたは短期のコルチコステロイド療法でうまく治療された
-
1名の患者は試験登録の数ヶ月前からMethotrexateの投与開始となったが、関節炎再燃の頻度は減らなかった
-
数十年にわたり、この患者群の関節炎症状はoligoarticular joint flares少関節炎というパターンに発展し、その頻度は時間とともに減少していった
-
すべての患者さんが1年に3〜4回の関節炎の症状を起こしている
-
診察時にこれらの発作で臨床的に最もよく侵される関節はMCP、PIP、DIPである(下図)
-
典型的には、患者は臨床的にDIP、PIP、MCP、MTP関節の重度の変形性関節症様の変化を認め、紅斑や圧痛を伴わない
-
Heberden結節、Swan neck変形、Boutonniere変形、手の尺側偏位を認めた
-
患者の一部では手首の可動域の減少とともに、第1手根骨関節の基部の扁平化を認めた
-
痛みやこわばり、腫れや紅斑などの既往歴は、すべての患者で認めた
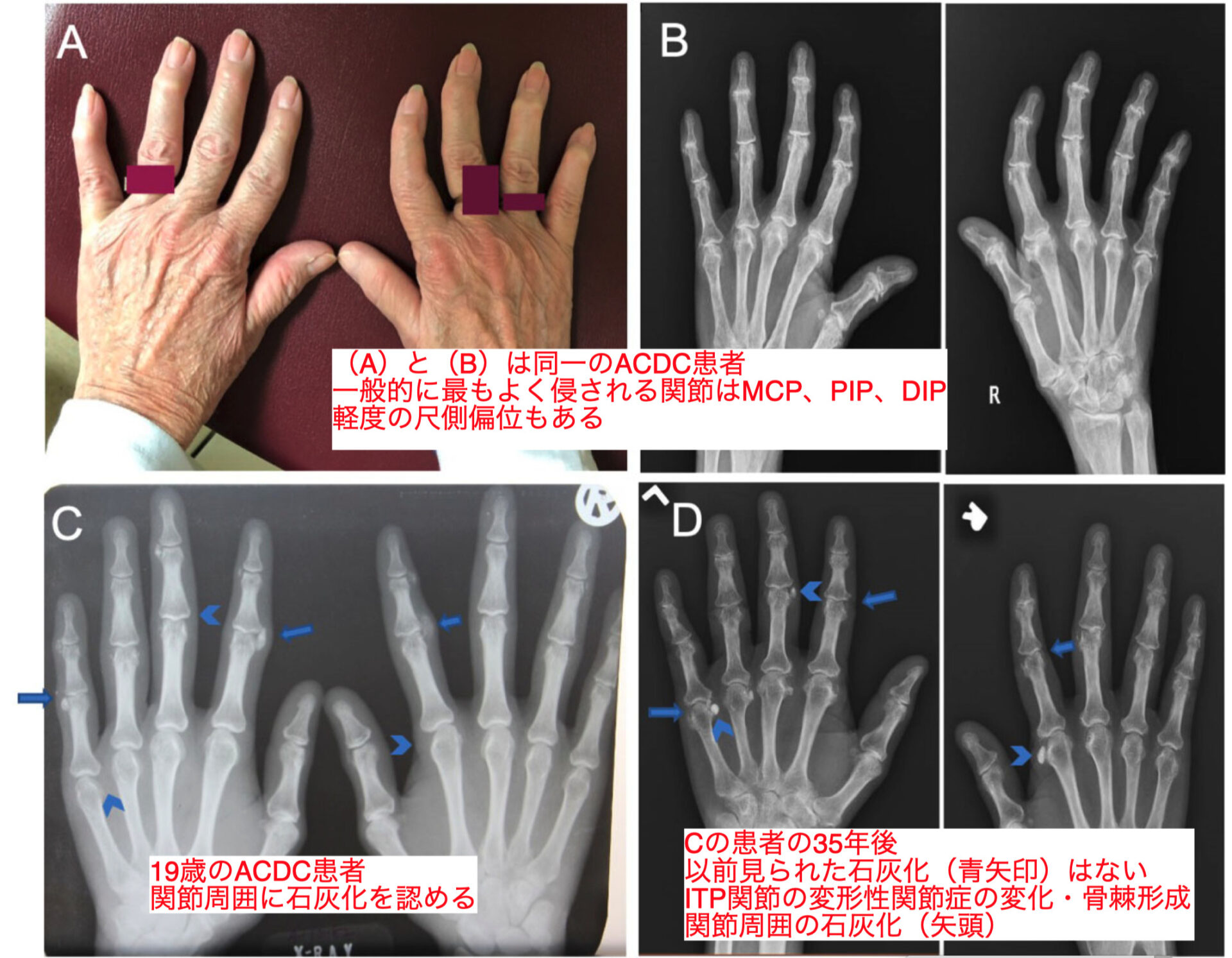
ACDC患者の主な放射線学的特徴
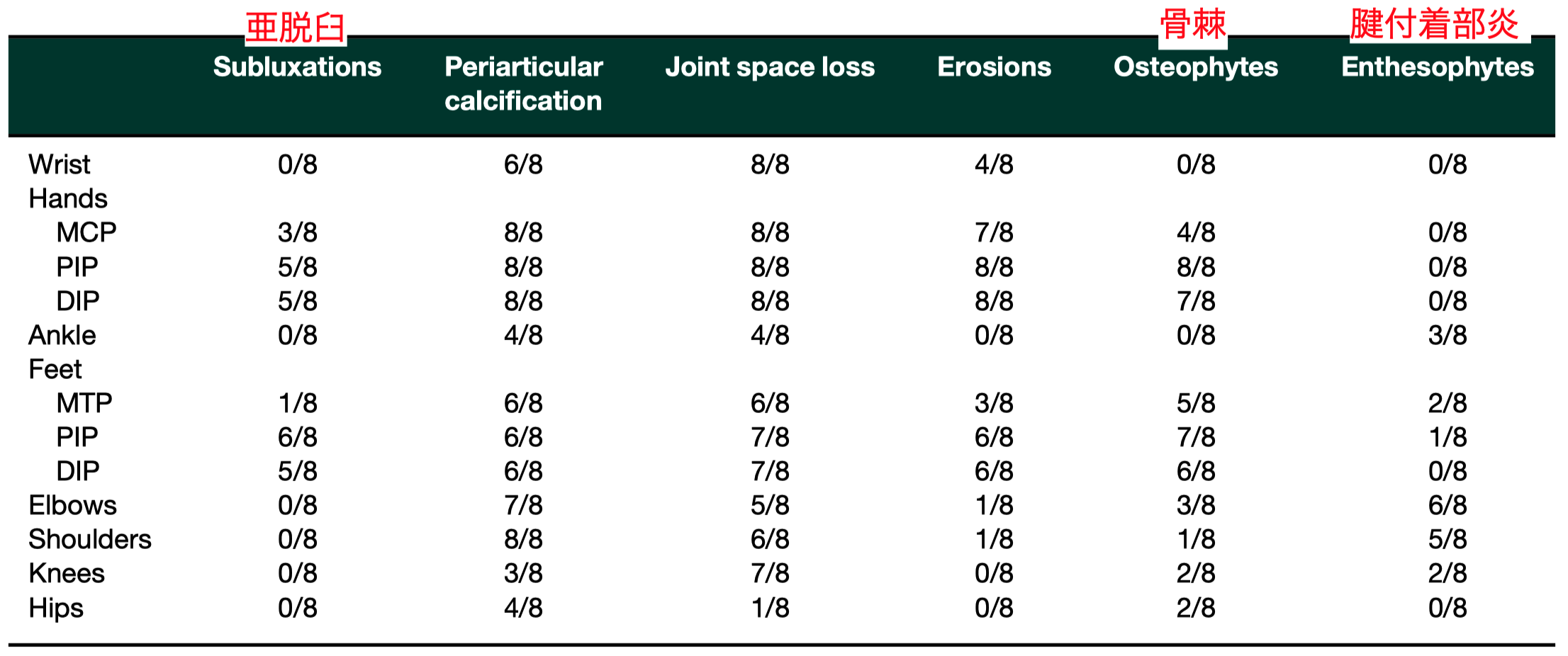
-
図1C→Dの35年後の変化では進行する石灰化と時間とともに退行する石灰化がある
-
図をみると3つの部位で石灰化は進行するが、他の3つの部位は減少している
-
つまり退行性骨棘とは非定型的な経過で進行した関節周囲の石灰化を認めている
-
-
X線写真とMRIでは、関節腔の減少や関節包と関節包周囲の石灰化、軟部組織の均質な石灰化、また侵食性の変性も確認できる
-
小関節のびらんは、関節窩やその周囲によく見られ、側副靭帯は石灰化していることが多い
-
生産的で治癒した骨変化もある
-
手根骨の侵食は時折認めたが、手首のtriangular fibrocartilage complex三角線維軟骨複合体の軟骨石灰化認めない
-
いくつかの症例では関節MRIにより、骨髄水腫を伴わない関節周囲のびらんの過程を確認することが可能
Radiographic axial involvement
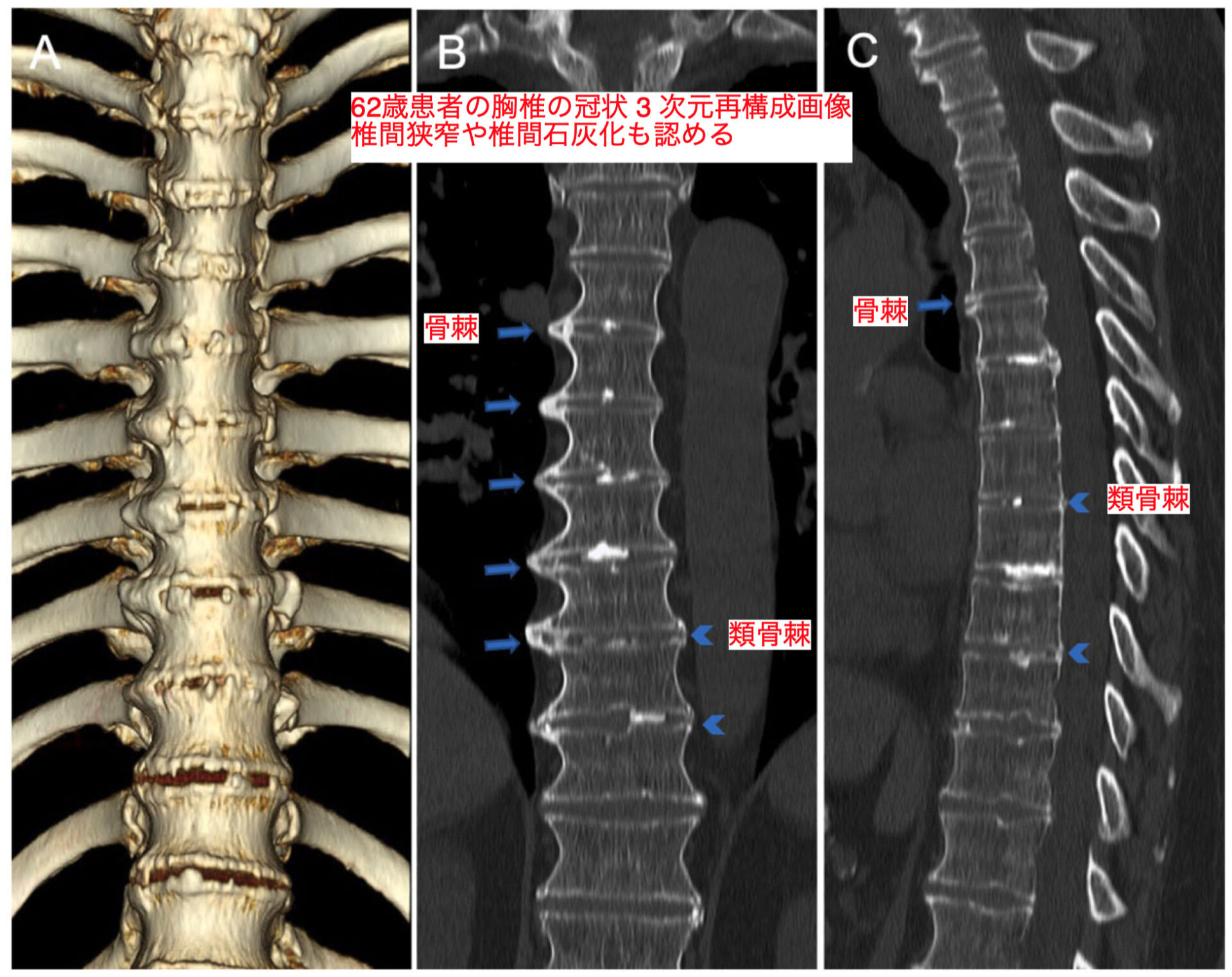
Vascular manifestations 血管の症状
- ACDC患者は、重度の下肢動脈大血管石灰化を呈して、腸骨動脈、大腿動脈、膝窩動脈、脛骨動脈に閉塞を引き起こし、広範な側副血行路を発達させる
- 動脈石灰化過程の発症は不明であるが、患者は典型的には30代で症候性跛行を発症する
- 4人の患者には跛行の悪化や切迫した虚血のために、大腿外科バイパス術やステント留置術を必要とした
- 他の血管床に関しては、それほど広くはない無症状な石灰化が観察された
- bypass手術のサンプルをX線マイクロトモシンセシスとX線回折で分析したところ、hydroxyapatite crystalsハイドロキシアパタイト結晶が血管石灰化の主成分であることが判明した
- サンプルを組織学的に解析すると、arterial wall thickening動脈壁の肥厚と、lamina elastica interna内弾性膜に、fragmentation of the elastin fibresエラスチン線維の断片化とともに重度の石灰化を認めた
検査所見と病理所見
- すべての患者はRF・抗CCP抗体・ANAが陰性で寛解期には炎症マーカーは正常であった
- 血清カルシウム値、リン酸塩、アルカリホスファターゼnikannsitemo
- 正常範囲内であった
- 4人のACDC患者から滑膜組織と体液の検体を採取したが、関節周囲の石灰化に隣接するMCP関節も変形性関節症の変化を呈しており(最初の図のBとDを参照)、X線写真では、すべての石灰化は数年前から存在していた
- 滑膜生検サンプルの組織学的検査で、dense fibrocartilaginous高密度の線維軟骨とコラーゲン組織が検出され、2/4サンプルで2つでspherical microcalcifications球状微小石灰化を、1つのサンプルでpyrophosphate-like calcifications ピロリン酸塩様石灰化を認めた
- 他の2つの生検サンプルでは石灰化のVon Kossa染色は陰性であり、炎症細胞は認められなかった
- しかしそのうち1つの生検サンプルでtumoural calcinosis腫瘍性石灰化症に似た石灰化を伴うhistiocytic reaction組織球性反応を認めた Am J Surg Pathol 2007;31:15–25.
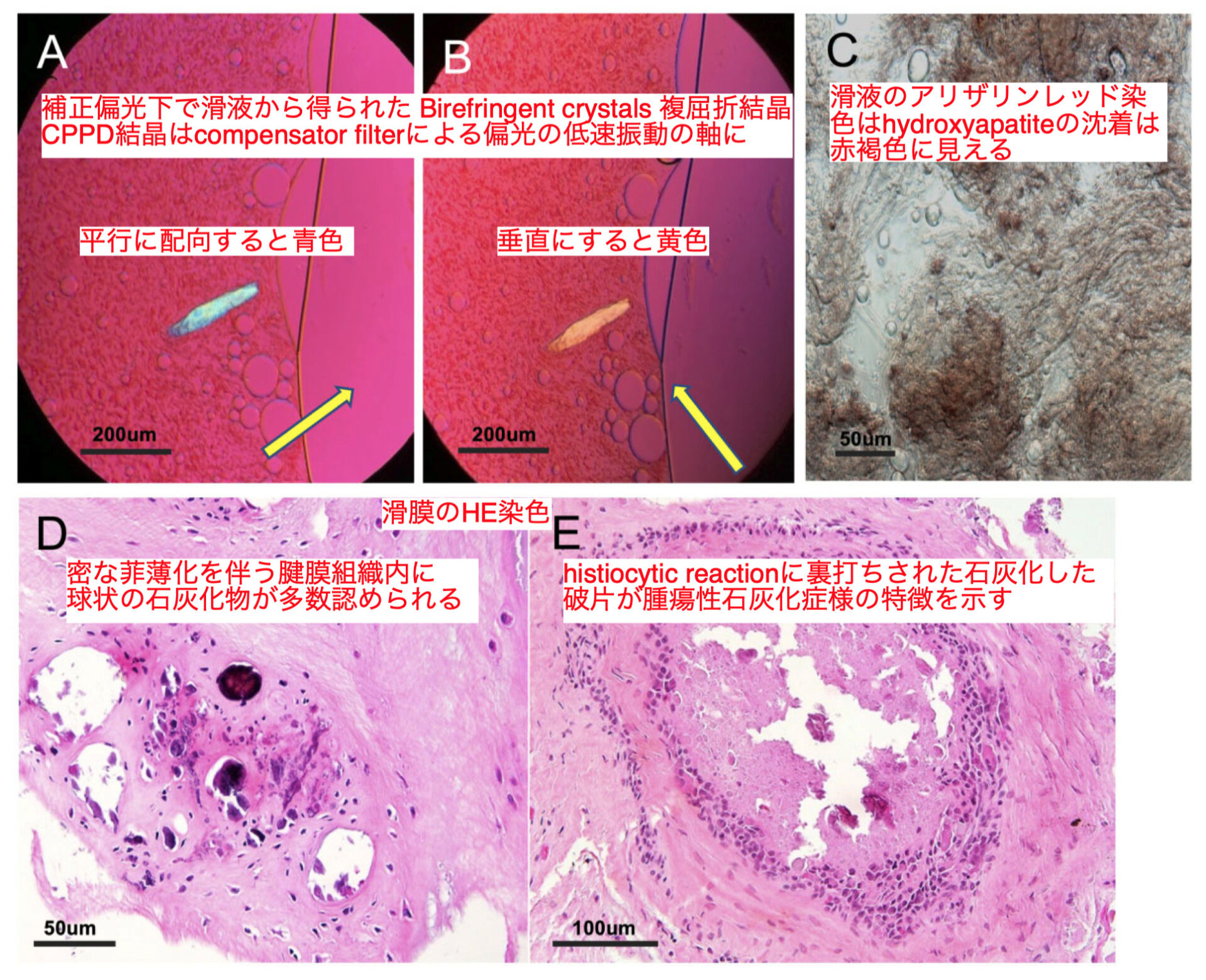
- オペ中に採取した滑液ではCPPDの血症あh確認されたが、尿酸血症はなかった
- 滑液のアリザリンレッド染色は4名とも強陽性で、basic calcium phosphate塩基性リン酸カルシウムまたはcalcium hydroxyapatite crystalsカルシウムヒドロキシアパタイト結晶の存在が示唆された
- 一方で滑膜組織中のbulk mineral depositsと同じ患者の以前に採取された血管石灰化サンプルは、X線回折研究により、ほとんどがハイドロキシアパタイト結晶であることが確認されたが、ピロリン酸カルシウム(CPP)の結晶は同定されなかった Radiol Case Rep 2020;15:1883–6.

【議論】
多くの症状は炎症性関節炎(RAやJIAなど)と誤診されることが多いが、今回RAとも典型的な結晶誘発性関節症とも異なる関節炎のパターンを同定した。主な特徴は以下の通り
-
発症年齢が若く、初期症状はepisodic arthritis周期性関節炎で、慢性症状は進行していく
-
大・小関節で時間とともに増減する複数の関節周囲石灰化病変を認める
-
手足に影響する侵食性の関節変化へ派生していく
-
osteoarthritic-appearing changes骨関節炎様変化を伴う頚椎と胸椎の病変を認める
-
関節周囲石灰化の部位では、組織学的に非炎症性である
- その他RF、抗CCP、ANAは陰性であり、自己免疫疾患の兆候もない
- カルシウムの沈着は主に関節包内と関節周囲に観察されたが、観察された変性性関節疾患とびらん性関節疾患の両方の特徴が混在する
- 一次性または二次性の内在性関節損傷が起こることが示唆された
- 腰椎のaxisの画像をとることで、脊椎靭帯や関節の骨化を伴い、DISHを想起させるような石灰化病変を有する Clin Anat 2016;29:870–7.
- 一方で、4つ以上の連続した椎体に病変があるが、患部の椎間板腔の狭小化や大きな椎間板石灰化の存在により、DISHと分類されるResnick and Niwayama and Utsinger基準を満たさないものがあった Semin Arthritis Rheum 1978;7:153–87.
- ACDC患者の脊椎画像には仙腸関節の関与はなかった
ACDC患者における石灰化の機序
- CD73 はecto-5 0 -nucleotidase enzyme 活性を持ち、細胞外の AMP をadenosineおよび Pi に変換する
- 生理学的条件下では、stromal cells ストローマ細胞,リンパ球(B 細胞およびいくつかの T 細胞のサブセット)および内皮細胞を含む様々な細胞に発現している Am J Physiol Cell Physiol 2019;317: C1079–92.
- CD73の発現は低酸素状態や炎症状態において増加する Curr Med Chem 2018;25:2260–71.
- CD73変異のLoss-of-functionにより以下が起こる
- 細胞外のadenosineおよび Pi の減少
- アルカリホスファターゼ活性の代償的アップレギュレーション
- P iの増加および石灰化形成の促進
NT5E Mutations and Arterial Calcifications. N Engl J Med 2011; 364:432–42.
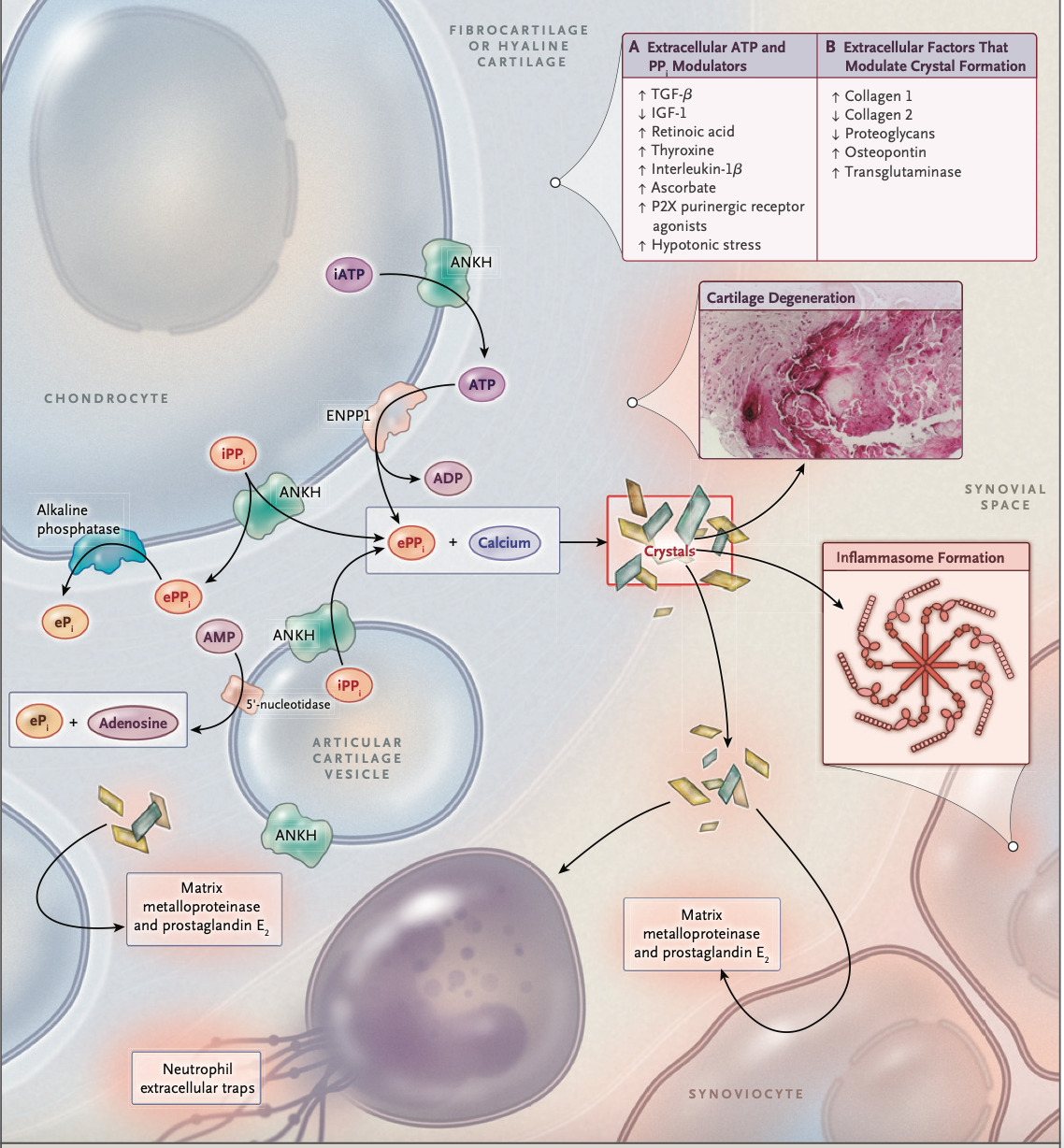
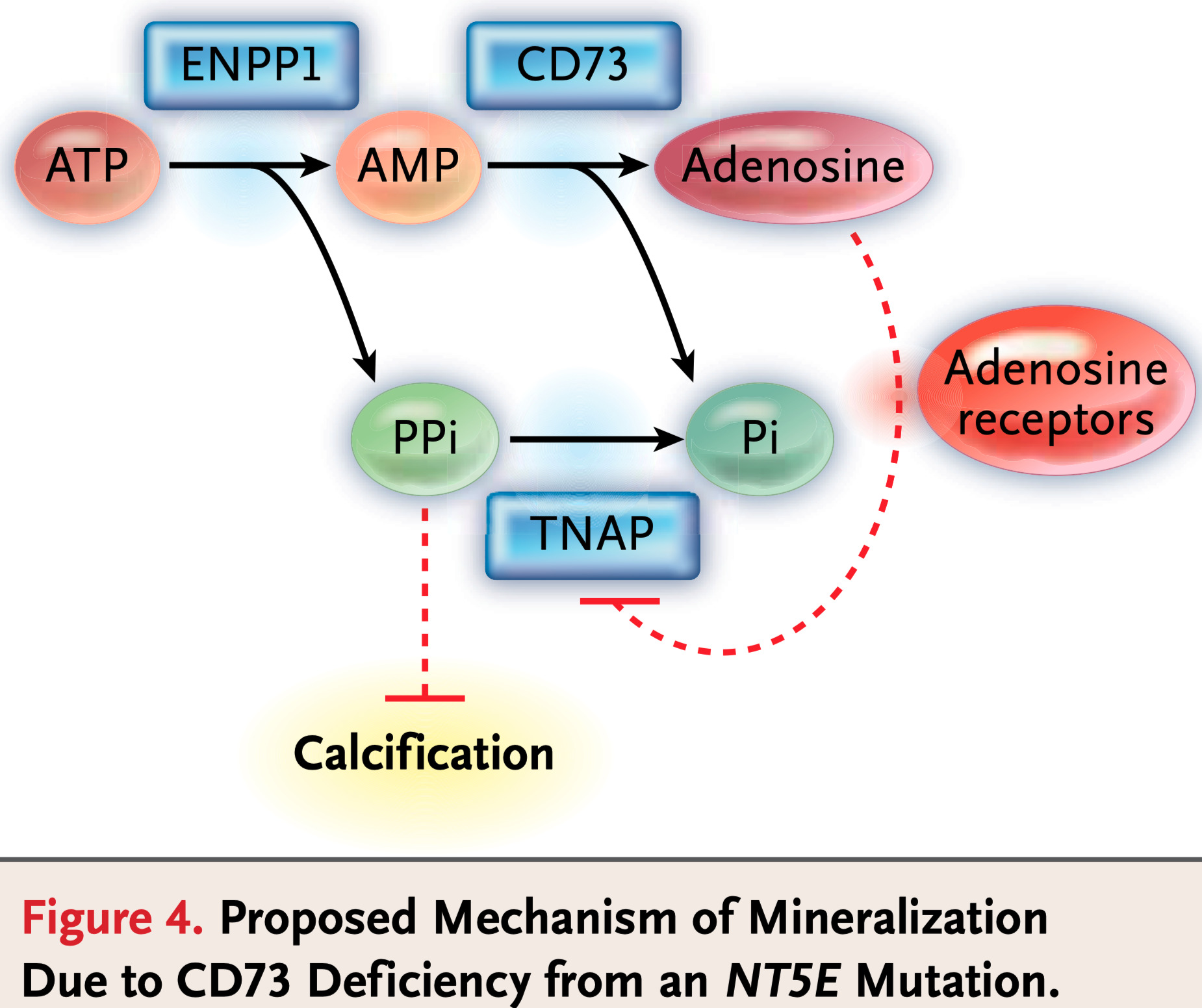
- ACDC患者における関節炎を引き起こす別の潜在的なメカニズムは、adenosineが局所的な欠乏するための考えられる Nat Rev Rheumatol 2017;13:41–51.
- adenosineは複数の細胞(内皮、血管平滑筋細胞および血小板)から放出され、脈石灰化の内因性阻害因子として機能する Cardiovasc Diagn Ther 2018;8:568–80.
- adenosine 2B receptors (A2B R) のアクチベーターによる治療は石灰化を抑制することができる Sci Signal 2016;9:ra121.
- MTXは細胞内アデノシン濃度を増加させるが、それではACDC患者の関節炎は効果的に制御できないかもしれない Joint Bone Spine 2019; 86:301–7.
- これはMTXの薬効では、CD73欠損によるアデノシンの生理的損失を補うには不十分である可能性がある