
NUDT15 gene variants and thiopurine-induced leukopenia in patients with inflammatory bowel disease. Intest Res. 2020 Jul; 18(3): 275–281.
【結論】
- アジア人におけるThiopurineチオプリン製剤で最も懸念される重度の白血球減少と脱毛はNUDT15 R139C遺伝子変異でほぼ完全に予測可能である。
- NUDT15遺伝子変異のスクリーニングはInflammatory Bowel Disease:IBD潰瘍性大腸炎の分野における個別化医療の重要な成功例である
- 一方、Thiopurineチオプリン製剤の他の副作用である肝障害、膵炎、リンパ腫などのは、NUDT15変異体では防ぐことができないため、さらなる研究が必要である
【背景】
-
プリン体アナログである6-mercaptopurine (6-MP) 6-メルカプトプリンには免疫抑制作用がある。Blood 1953;8:965-999.
-
6-MPのプロドラッグであるazathioprine (AZA) アザチオプリンは1966年からIBDで使用されている。Proc Soc Exp Biol Med 1958;99:164-167.
-
現在も寛解維持療法に使用されており、最近でもモノクローナル抗体療法における抗薬物抗体の産生を抑制するために使われており、自己免疫性肝炎や全身性エリテマトーデスの治療にも使用されている。
-
欧米人では骨髄抑制の発生率は3%であるが、J Crohns Colitis 2015;9:191-197.
-
アジア人では白血球減少のような重大な副作用が多く、15-40%で起こりやすいと言われており、Medicine (Baltimore) 2015;94:e1513.
-
投与開始後早期でも1%の患者に重度の白血球減少が発生する。J Gastroenterol 2016;51:22-29.
-
AZAの投与量は欧米のガイドラインでは2~2.5mg/kgで推奨されているのに対し、Gut 2019;68(Suppl 3): s1-s106.
-
アジアのガイドラインでは25mgの低用量の開始が推奨されている J G troenterol 2018;53:305-353.
-
欧米人では、チオプリンの代謝酵素の1つであるthiopurine S-methyltransferaseチオプリンS-メチルトランスフェラーゼ(TPMT)のgene variants遺伝子変異(TPMT*2、*3A、*3B、*3C)が白血球減少と関連していることが知られており、TPMT遺伝子変異に応じてチオプリンの投与量を調整することが推奨されている Clin Pharmacol Ther 2019;105:1095-1105.
- 2014年に、韓国のIBD患者を対象としたゲノムワイド関連研究により、nudix(nucleoside diphosphate-linked moiety X)type motif 15(NUDT15)またはnudix hydrolase 15(正式名称)遺伝子の変異がチオプリンによる早期白血球減少と関連していると報告された Nat Genet 2014;46:1017-1020.
- この変異体(rs116855232)は、タンパク質の139位のアルギニンをシステインに置き換える(R139C; p.Arg139Cys; c.415C>T)ものである
- またほぼ同じ時期にこのNUDT15遺伝子変異とチオプリンによる急性重症白血球減少症との相関が、日本人の急性リンパ性白血病患者で報告された Br J Haematol 2015;171: 109-115.
【チオプリンの代謝】
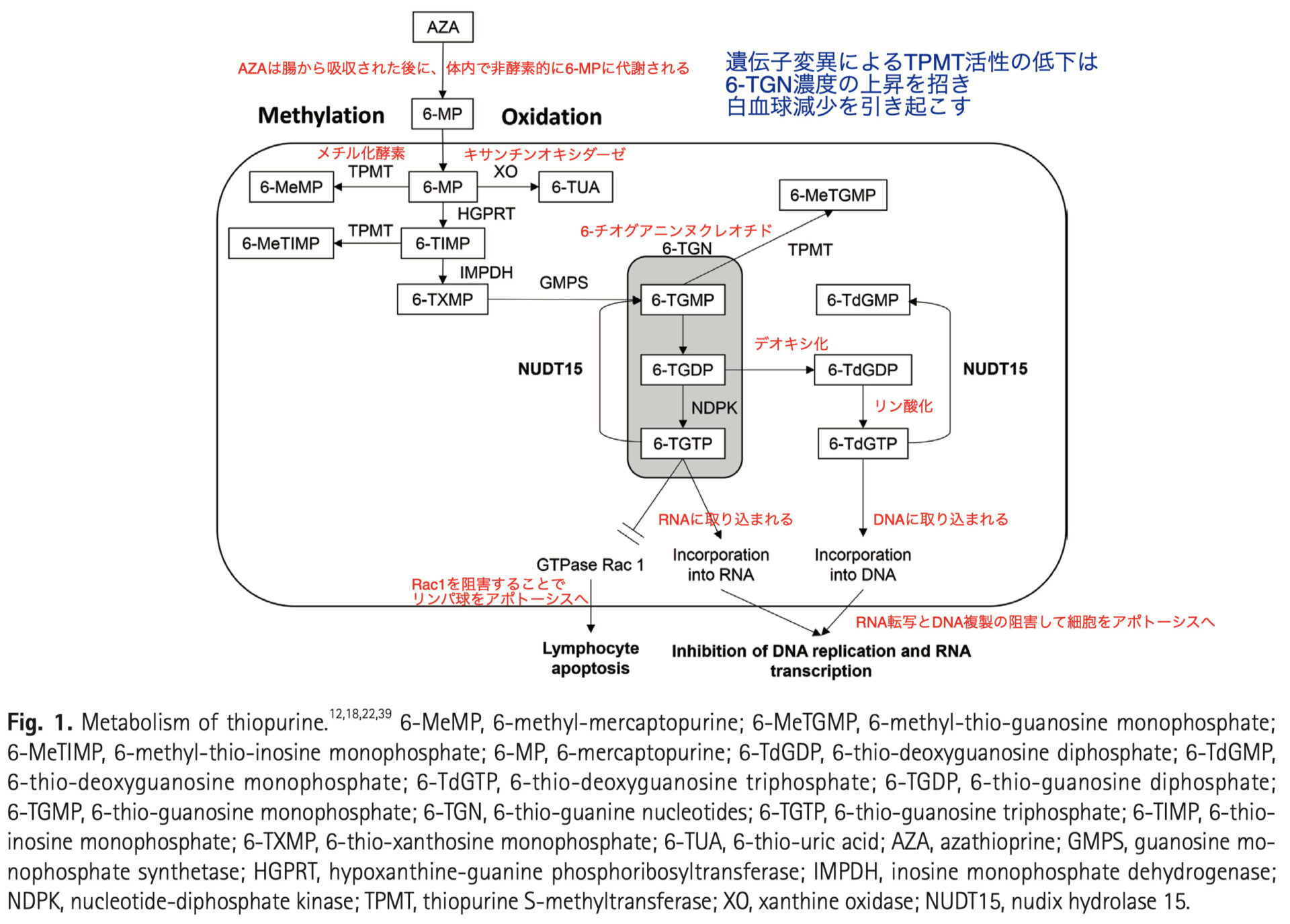
【NUDT15 の役割】
- NUDT15は6-T(d)GTPを6-T(d)GMPへの加水分解酵素である (Fig.1)
- NUDT15遺伝子は3つのエキソンからなり、高度に保存されたNUDIXボックスを持つNUDIXヒドロラーゼファミリーに属し、任意の部位に好適なヌクレオシド二リン酸をヌクレオシド一リン酸に加水分解する Leuk Res 2017;62:17-22.
- 他のNUDIXファミリータンパク質とは異なり、NUDT15タンパク質はホモ二量体を形成する Nat Commun 2015;6:7871.
- NUDT15 R139C変異体は、触媒部位の安定化を阻害し、タンパク質の構造変化を引き起こす Biochim Biophys Acta Proteins Proteom 2019;1867:376-381.
- NUDT15遺伝子に変異があると、その酵素活性が低下し、6-TGTPおよび6-TdGTPのレベルが増加する。これらはそれぞれRNAとDNAに取り込まれ、白血球減少を引き起こす (Fig.1)
- これらの結果は、6-TGN が 6-TGMP、6-TGDP、6-TGTP をまとめて測定するため(Fig.1)、NUDT15 R139C 遺伝子変異が 6-TGN レベルと相関しないことを説明できる。
- in vivo では、NUDT15ノックアウトマウスに6-MPを投与すると 6-TdGTP の DNA への組み込みが増加した Blood 2018;131:2466-2474.
- ヒトの NUDT15 R139C 変異に対応する相同変異を持つマウスでは、高用量の 6-MP (2 mg/kg) が造血幹細胞および前駆細胞を損傷し、致死性の白血球減少を引き起こす Leukemia 2020;34:882-894.
- NUDT15 はチオプリンの代謝に重要な酵素であるが、生体内での生理的機能はまだ不明である。NUDT15は、酸化ストレスによって生成される最も一般的な酸化的dNTPの一つで、DNA合成の強力な変異原性基質である8-oxo-dGTPを、8-oxo-dGDPまたは8-oxo-dGMPに加水分解できる Biochem Biophys Res Commun 2003; 305:1073-1077.
- しかしNUDT15の枯渇は生体内のDNAへの8-oxo-dGTP組み込みに影響がないことから、この効果の重要度は小さいと考えられている Nat Commun 2015;6:7871.
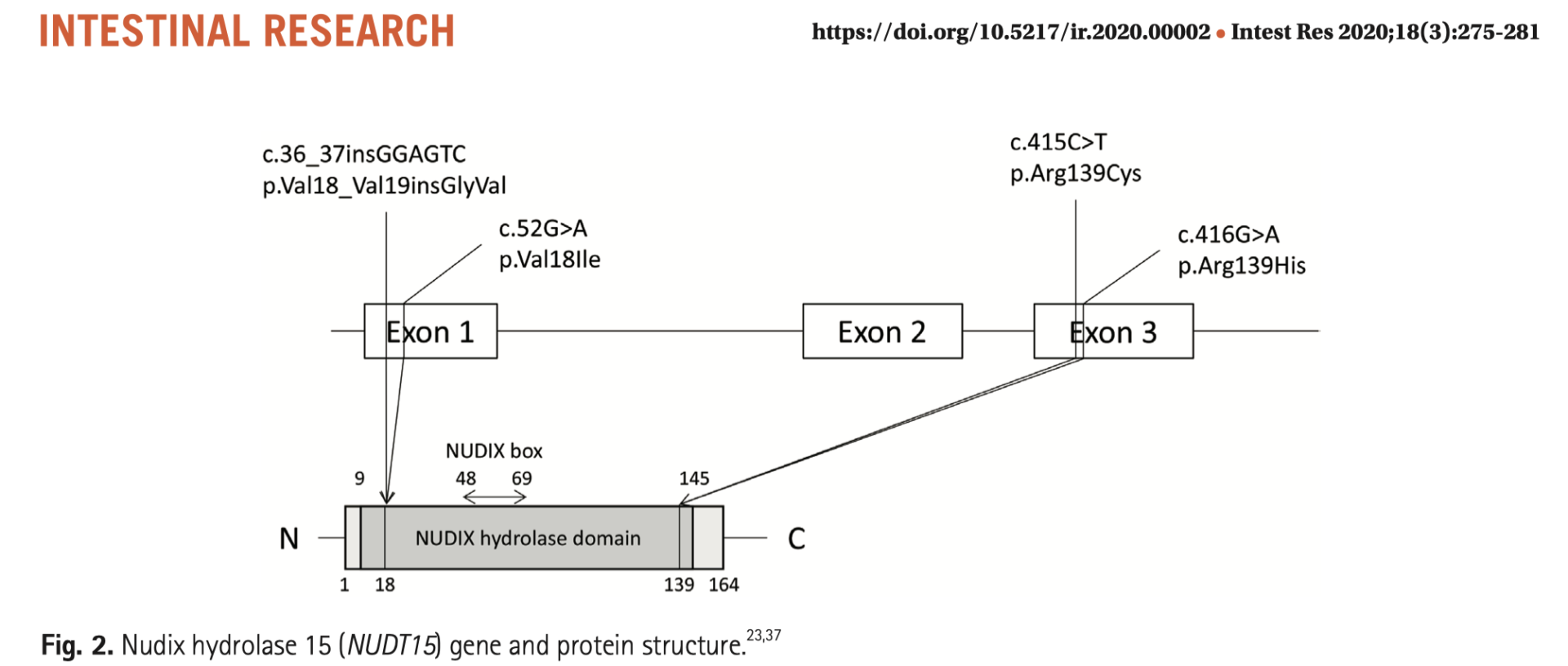
【Nudt15遺伝子変異の頻度】
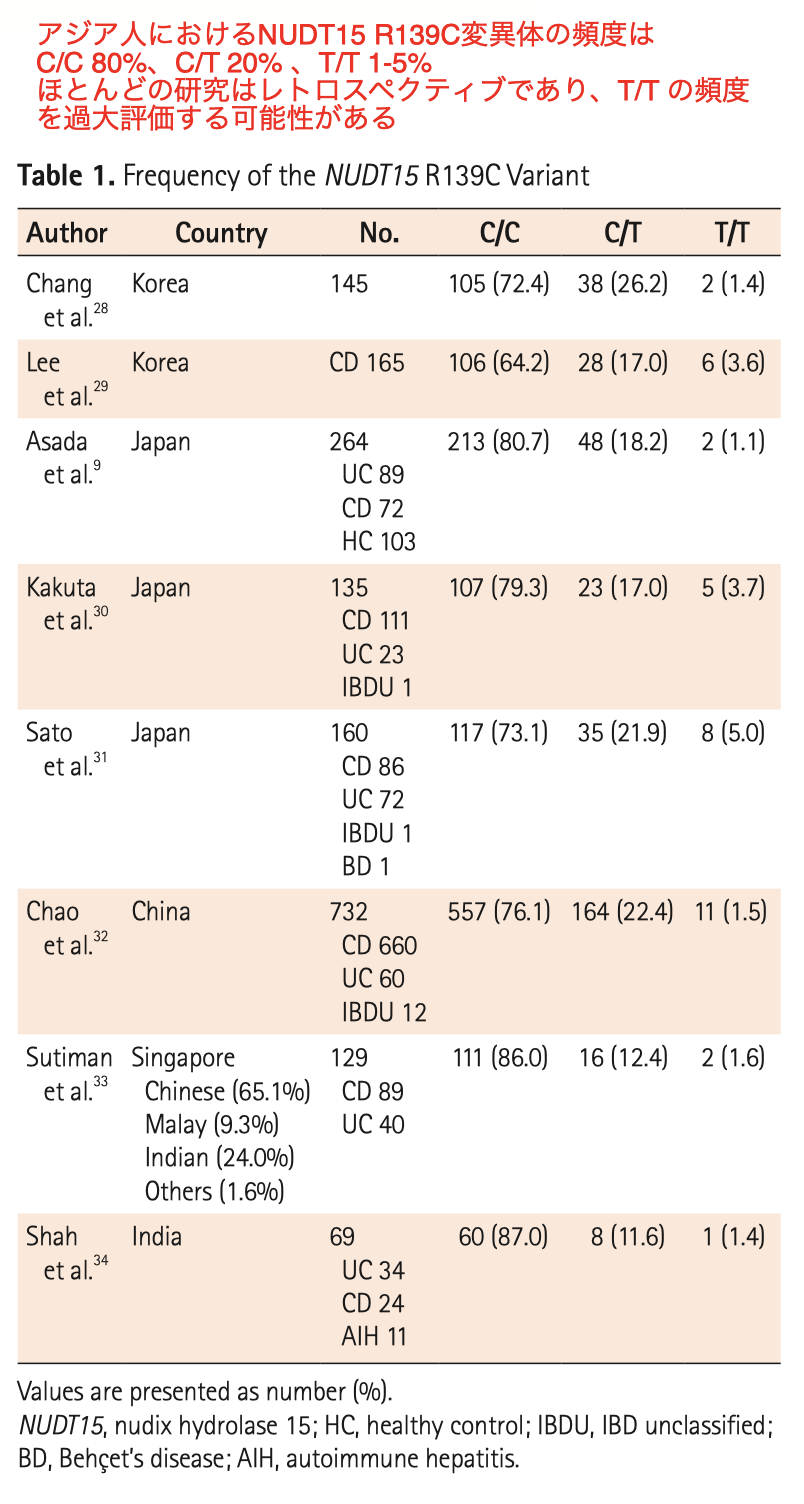
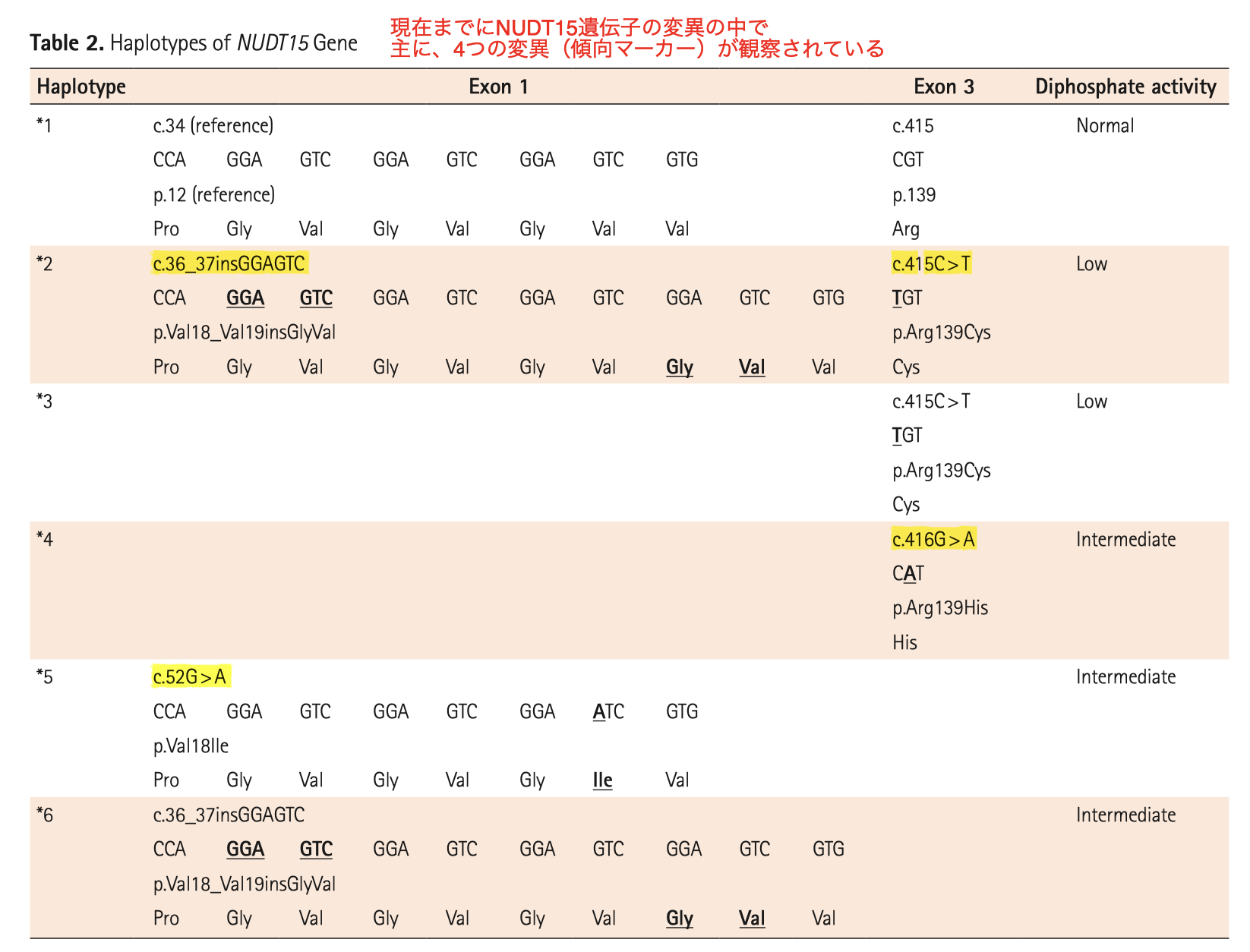
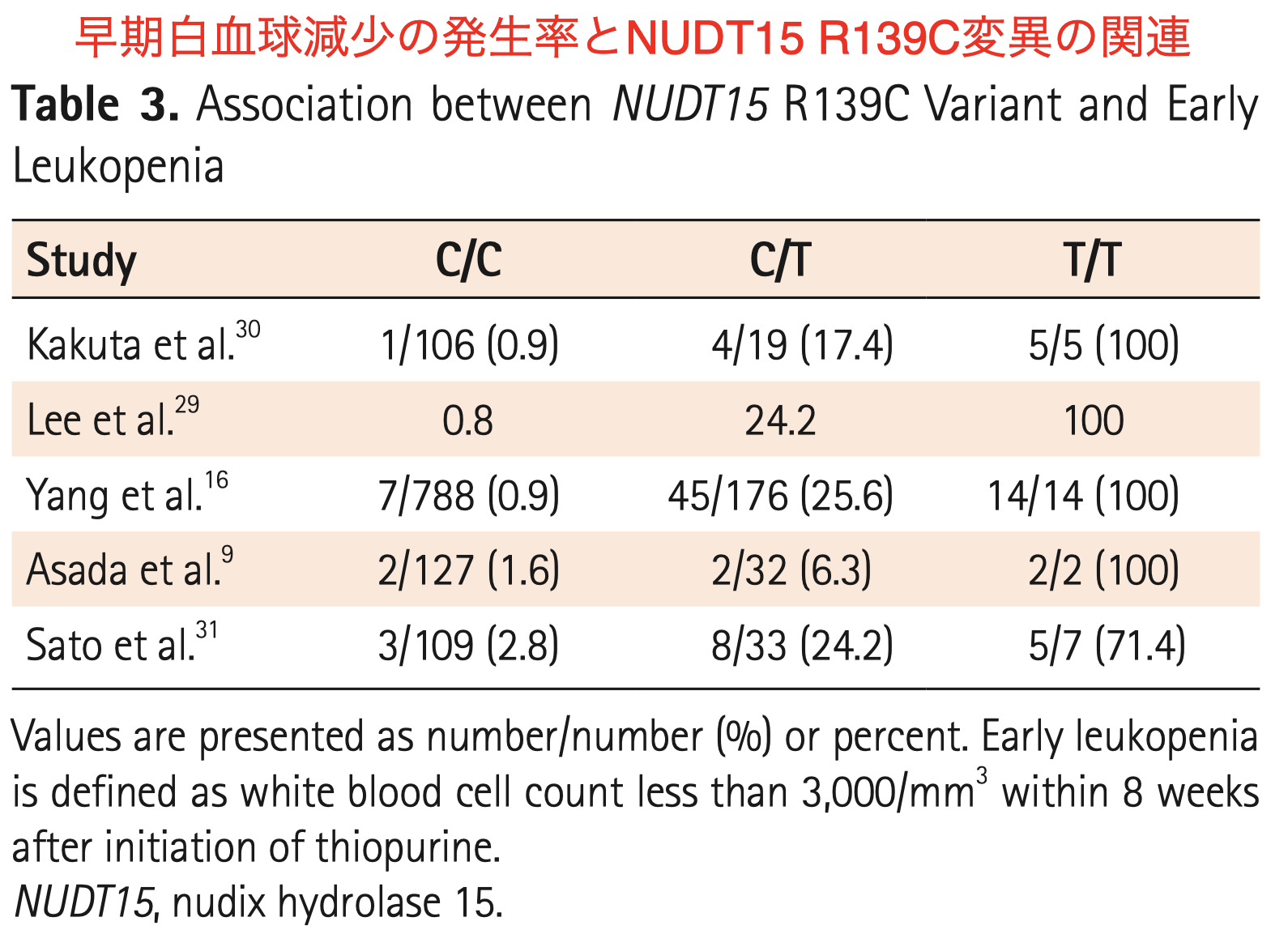
【チオプリン誘発性早期重症白血球減少症とNudt15遺伝子変異】
チオプリン投与開始後8週間以内の白血球数が3,000個/mm3未満を早期白血球減少と定義した研究
- 早期白血球減少はC/Cの患者では3%未満、C/Tでは約20%、T/Tではほぼすべての患者に発生した。
- R139C 変異体に加え、中国のグループは c.36_37insGAGTC と c.52G>A 変異体も白血球減少と関連し、これらの変異体の組み合わせにより白血球減少をより正確に予測できると報告している Inflamm Bowel Dis 2017;23:1592-1599.
- チオプリン投与前にNUDT15 R139C遺伝子変異を測定することの有用性を報告した韓国の前向き研究 Clin G ol Hepatol. [published online ahead of print August 22, 2019]. https://doi.org/10.1016/j.cgh.2019.08.034.
-
182名のIBD患者が、azathioprineアザチオプリン投与前に遺伝子検査(NUDT15, FTO [fat mass and obesity-associated protein], TPMT)を受ける群と受けない群に無作為化
-
azathioprine 50 mgから開始し、patients with no genetic variant in the genotyping group遺伝子型判定群では遺伝子変異のない患者、those in the non-genotyping group.非遺伝子型判定群では2.0~2.5 mg/kgまで徐々に増量した。
-
いずれのrisk variantも homozygousホモ接合体である患者 には、azathioprineの投与は推奨されず
-
試験期間中の骨髄抑制の発生率は,非遺伝子型判定群では遺伝子型判定群に比べ有意に高かった(35.9% vs. 16.7%)
-
白血球減少症の多くはThe heterozygous NUDT15 variant(NUDT15ヘテロ接合型バリアント) が原因との結論づけ
-
これらの研究の蓄積により、NUDT15遺伝子変異は、チオプリン投与前に実施すべき検査として最近のガイドラインに記載されている。
- 日本では、2019年2月にNUDT15 R139C変異の測定が臨床使用として承認。
-
チオプリンはT/Tの患者には禁忌
-
C/Tの患者における最適な投与方法は未確定
-
- 日本の大規模多施設共同レトロスペクティブ研究 J G terol 2018;53:1065-1078.
-
C/TまたはT/Tの患者では、C/Cの患者よりも白血球減少までの時間が短く、チオプリンの耐doseも少ない。
-
- 他の研究では、この変異を持つヘテロ接合体の患者では、この変異を持たない患者よりも白血球数と血小板数の減少が長く(最大6ヶ月)持続することが示されており、このような患者では、白血球数の長期にわたる慎重なモニタリングが必要 J G ol Hepatol 2019;34:1751-1757.





