
Management of Aromatase Inhibitor–Induced Musculoskeletal Symptoms. JCO Oncol Pract. 2020 Nov;16(11):733-739.
【INTRODUCTION】
- 最初のaromatase inhibitor (AI)アロマターゼ阻害剤であるanastrozoleアナストロゾールが承認され、閉経後女性のホルモン受容体陽性乳癌の治療・予防に使用されてきた Breast Cancer Res Treat 140:233-240, 2013
- 2000年にanastrozole と tamoxifenのefficacyを検討した研究では両剤の副作用として関節痛は特に言及されなかった
- しかしながら、研究者らは、どちらの治療を受けている女性でも約8%が一般的な痛みを、特に6%が骨の痛みを報告していることに着目している J Clin Oncol 18:3748-3757, 2000
- 翌年、AI-induced musculoskeletal symptoms (AIMSS)AIによる筋骨格系症状が初めて明確な有害事象として報告された J Clin Oncol 19:2767, 2001
- 以後はAIMSSはAI治療の重大な毒性として認識されるようになっている Breast Cancer Res Treat 111:365-372, 2008
【NATURAL HISTORY OF AI ARTHRALGIA】
Presentation and Prevalence
-
AIMSSはprotean presentation変幻自在なプレゼンテーションをとる
- 一般的には関節痛とstiffnessこわばり J Clin Oncol 25:3877-3883, 2007
- 以下のような場合もある
- carpal tunnel syndrome(CTS) J Clin Oncol 34:139-143, 2016
- tenosynovitis
- myalgia
- muscle weakness J Clin Oncol 26:3147-3152, 2008
- 症状:継続的または断続的
-
部位:中枢の関節や末梢の関節療法いずれも関与している
-
時期:AIMSS発現期間の中央値は約6週間であるが、AI投与中はいつでも症状が発現する可能性がある
- 症状がピークに達し、AIMSSのためにAIを中止するまでの期間の中央値は約6ヵ月である Breast Cancer Res Treat 111:365-372, 2008
-
A systematic review and meta-analysisではAIMSSのprevalenceは20~74%。pooled prevalenceは46% Support Care Cancer 25:1673-1686, 2017
-
Intergroup Exemestane Studyではexemestaneエキセメスタン(第3世代アロマターゼ阻害薬)投与中の女性の2.8%がCTSを発症し、その半数 は両側性であった
-
一方、タモキシフェン投与中にCTSを発症した女性は、わずか0.3%
Clinicopathologic Associations With AIMSS AIMSSと臨床病理学的関連性
-
AIMSSの予測因子は研究されているが、ほとんど一貫性のある関連はない Support Care Cancer 25:1673-1686, 2017
-
例外としては、the last menstrual period (LMP)閉経からの期間の研究で、AIMSSの発生率5年以内にLMPを迎えた女性ではは45%-73%であり、10年以上たっている場合は25%-75%であった BMC Cancer 11:436, 2011
-
閉経による近年のエストロゲンの減少が、AIによる循環エストロゲン濃度のさらなる低下と相まって、症状を悪化させる可能性があると考えられている
-
- その他関連する可能性があると考えられている因子は以下の通り Support Care Cancer 25:1673-1686, 2017
- body mass index (BMI)
- prior taxane chemotherapy タキサン系の化学療法歴
- prior tamoxifen therapy タモキシフェンの治療歴
- stage of cancer
Mechanism
-
AIMSSのメカニズムは完全には解明されていないが、エストロゲン欠乏と関節炎との関連は研究されている
-
Menopausal arthritis閉経期関節炎は中年女性に発症する慢性多発性関節炎で閉経期またはその直後に発症する
-
最近の研究では、女性の約半数が閉経前後に関節の痛みやこわばりを訴えている Post Reprod Health 24:34-43, 2018
-
estrogen deprivationエストロゲン欠乏に伴う関節症の病態には、正常なエストロゲンとエストロゲン受容体の相互作用の破綻に伴う分子レベルの変化の関与している可能性がある
- エストロゲン受容体は核内ホルモン受容体であり、炎症性サイトカインを含む様々なタンパク質の発現を制御している Breast Cancer Res 17:89, 2015
- 例えば、活性化されたエストロゲン受容体は炎症性サイトカインであるIL-6やTNFaの発現を抑制するが、これらの濃度は閉経後の上昇する Endocr Rev 23:90-119, 2002
- エストロゲン受容体は核内ホルモン受容体であり、炎症性サイトカインを含む様々なタンパク質の発現を制御している Breast Cancer Res 17:89, 2015
-
AIMSSと疲労および不眠症の間に関連性を見いだした研究では、C-reactive protein, eotaxin, monocyte chemoattractant protein-1, and vitamin D binding proteinなどの炎症性マーカーのレベルが上昇していることが報告されている Breast Cancer Res 17:89, 2015
-
SNIPの関与も同定されており、このSNIPが T-cell leukemia 1A T細胞白血病1A遺伝子と関連や、この遺伝子自体が炎症性サイトカイン受容体IL-17RAの発現と関連しているとも報告されている J Clin Oncol 28:4674-4682, 2010
- AIの局所炎症作用は、画像検査の変化から示唆されている
- tamoxifen と AIを投与された17名の女性での研究でベースラインと6ヶ月後に握力測定と手/手首のMRIを実施
- AIを投与された女性は、握力の有意な低下とMRI上の有意な腱鞘炎の変化およびその相関性も認めた
- タモキシフェンでは、このような変化はほとんどなし
Do AIMSS Predict Improved Breast Cancer–Related Outcomes?
- AIMSSが乳がん関連の転帰の改善を予測するかどうかは、prospectivelyには評価されてretrospectivelyでは矛盾した報告がある。
- ATAC試験やTamoxifen Exemestane Adjuvant Multinational(TEAM)試験、Intergroup Exemestane Studyなどが報告されているが、AIMSSが乳房症状の改善を予測するのに役立つかどうかは不明
【MANAGEMENT】
いくつかの臨床試験あるが、only single-arm studiesか小規模なplacebo-controlled studyであり、限られている。
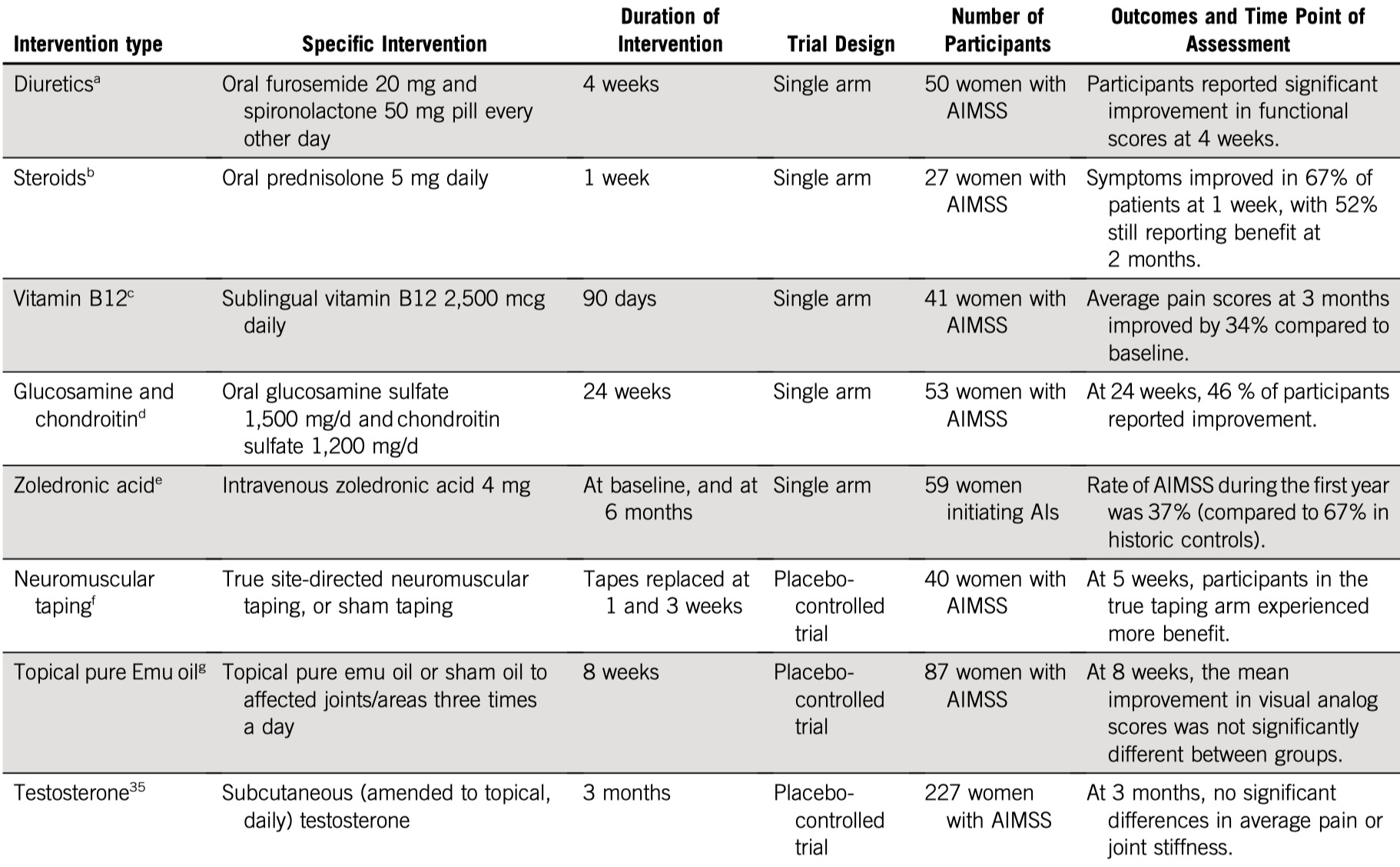
しかし、より広範に評価された有効な治療法がある(以降に記載)ため、上記のアプローチは推奨されない
【GENERAL PRINCIPLES】
Symptomatic Treatment 対症療法
- アセトアミノフェンや非ステロイド性抗炎症薬(NSAIDs)は短期間は有用かもしれないが、慢性使用は推奨されない
- オピオイドはAIMSSの治療には推奨されない
- 予防運動、モニタリング、および症状の報告に関する患者教育が推奨
Site-Directed Therapy 部位別治療
-
AI使用によりCTSやトリガーフィンガーを発症した患者の場合、一般的な症状は軽度である
-
ATAC試験では、CTSを発症した患者80名のうち、何らかの介入を必要としたのは18名のみ J Clin Oncol 27:4961-4965, 2009
-
-
必要に応じて、手根管開放術やトリガーフィンガーのステロイド注射の選択肢もある
-
またCTS患者には夜間スプリントを使用することができる
【MODALITIES TO TREAT AIMSS】
Omega-3 Fatty Acids
-
オメガ3脂肪酸(O3 -FA)は、関節痛の強さ、罹患関節数、こわばり、NSAID使用の減少に有効である
-
O3 -FA は肥満患者の AIMSS 治療に有用である
-
ある試験で、AIMSS女性患者249人が、O3 -FAs 3.3 gまたはプラセボ(大豆/コーン油)を毎日24週間ランダムに割り当てられた。ベースラインと比較して、12週目のAIMSS症状は群間に有意差はなし J Clin Oncol 33:1910-1917, 2015
-
しかし、BMI で層別化した事後解析では、O3 -FA 群の肥満患者 110 名(BMI ≧ 30 kg/m)でプラセボ群と比較して有意に低い疼痛スコアを示した Breast Cancer Res Treat 172:603-610, 2018
-
Exercise and/or Yoga Therapy
-
prospective trialではトレッドミルウォーキングや筋力トレーニングといった有酸素運動・抵抗運動を組み合わせることで、AIMSS症状の緩和させることが示された
-
The Hormones and Physical Exercise (HOPE) trialでは少なくとも軽度のAIMSSを経験したを経験し、adjuvant AIsによる治療を受けている運動していない女性121名を登録し、30名の参加者を運動群と通常ケア群に無作為に割り付け Cancer 125:2262-2271, 2019
-
12ヵ月後の関節痛のWorst joint pain scoresは、運動療法に無作為に割り付けられた女性では1.6ポイント減少できたが、通常ケア群では0.2ポイント増加した
-
1年後、運動群では、全体的なQOL、乳がん特異的・内分泌特異的・疲労特異的スコアで大きな改善を有した
-
重要なことは、この介入がfeasible実現可能であるということ
-
-
yogaヨガのPilot studiesでは、ヨガによってアウトカム(バランス、柔軟性、知覚障害、疼痛、QOL)が改善されることが示された Integr Cancer Ther 11:313-320, 2012
-
一方、他の試験ではプラセボ対照群でもAIMSSの比較的顕著な改善が見られることから、研究結果としてはいくつかの限界がある Cancer Res 79, 2019 (4 suppl; abstract P4-16-01)
-
それでも、すべての乳がん患者、特にAIMSSを有する患者に対して運動と身体活動を推奨することは妥当である
-
Acupuncture鍼治療
-
鍼治療は、変形性関節症など様々な症状の治療に用いられる人気の非薬物療法である
-
単施設無作為化比較試験では、真の鍼治療と偽の鍼治療を比較したところ、6週間後に痛みの重症度と疼痛関連の干渉が群間で有意に改善した J Clin Oncol 28:1154-1160, 2010
-
より大規模な多施設共同試験では、AIMSS女性患者226人を真の鍼治療と偽の鍼治療、コントロールに無作為にわりつけ JAMA 320:167-176, 2018
-
真性鍼療法と偽鍼療法では、30~45分のセッションを6週間かけて12回(週2回)行った
-
ベースラインから6週間後までの関節症状の改善度は、真の鍼治療群では約2ポイントであったが、偽の鍼治療群およびコントロール群では約1ポイントであり、群間効果は約1ポイントであった
-
post hoc analysisでは、真の鍼治療群では52%の患者がベースラインから30%の疼痛スコアの改善を達成したのに対し、偽の鍼治療群では33%、コントロール群では29%であった
-
つまり、真の鍼治療群の半数以上の患者が、痛みに対して“clinically meaningful”臨床的に意味のある反応を経験した
-
これらのデータは、AIMSS治療に鍼治療を使用することを支持する
-
-
Duloxetineデュロキセチン
-
デュロキセチンはSNRIでうつ病、不安神経症、fibromyalgiaのような慢性疼痛の治療薬として承認されている
-
単施設研究ではAIMSSの女性患者29人のうち21人(72%)が8週間後の平均疼痛が少なくとも30%減少した Cancer 117:5469-5475, 2011
-
Duloxetine’s utilityデュロキセチンの有用性を確認したより大規模な多施設間ランダム化比較試験がある J Clin Oncol 36:326-332, 2018
-
患者:AIMSSを有し、平均関節痛スコアが 4/10以上の患者299名
-
方法:デュロキセチン投与群(30mg/日を1週間、その後60mg/日を11週間、その後30mg/日を1週間)およびプラセボを13週間投与群
- デュロキセチン投与群では6週目に臨床的に意味のある改善(2ポイント)
- デュロキセチン投与群ではプラセボ群と比較して12週間にわたる関節痛の平均スコアで0.82ポイント低い
- あらゆるグレードの有害事象の発生率は、デュロキセチン投与群で高く(78%対50%)、グレード3の有害事象の発生率はそれぞれ9%と4%でその内訳は疲労(32%)、吐き気(30%)、口渇(25%)、頭痛(21%)
-
- デュロキセチン投与群では投与中止12週間以内で、疼痛スコアはプラセボと同等であった
- ここからは、病理学的なプロセスというよりは、analgesia鎮痛作用がある仮説が支持される
- またBMIが高い女性の方が、よりデュロキセチンが有効という報告があり、Omega-3 Fatty Acidsと同等の結果である Cancer 125:2123-2129, 2019
- 要約すると、デュロキセチンは治療した患者の約70%でAIMSSを減少させるが、中には耐え難い有害事象を経験する患者も認める
Vitamin D Therapy
-
ビタミンDに関するデータは さまざま
-
AIに伴うエストロゲン不足の状態は機能的なビタミンD不足を引き起こす可能性がある
-
機序としてはエストロゲンはビタミンDとその受容体の両方を活性化するので、機能的なビタミンD不足を引き起こす可能性がある
-
ビタミンD濃度とAIMSSの発症との相関は示されなかった Clin Breast Cancer 18:78-87, 2018
-
-
あるプラセボ対照無作為化試験では60人の参加者を高用量ビタミンD群とプラセボ群に無作為に割り付け Breast Cancer Res Treat 129:107-116, 2011
-
ベースラインの25-hydroxyvitamin D levelによって投与量を層別化
-
2ヵ月後、疼痛・機能のスコアは、ビタミンD補充群の方がプラセボ群より良好であった
-
しかし投与数が少なく、中止率が高かったため、解析は限定的であった
-
-
別の試験では、ベースラインの25-hydroxyvitamin D levelが40ng/mLであり、letrozoleレトロゾールの治療を開始した女性160人を登録
-
ビタミン D 群(カルシウム1,200mgとビタミンD3 600IUの標準サプリメントに加え、ビタミンD3 30,000 IUを週3回)、プラセボ群に無作為に割り付け
-
24 週間後の複合エンドポイントである AIMSS の達成率は、ビタミン D 群 37%、プラセボ群 51%であった Breast Cancer Res Treat 166:491-500, 2017
-
- 別のRCTでは、AIMSSの女性113人を対象に、600IUまでビタミンDレベルを正常化したあとに2種類の投与量で2群に分けた(600 IU v 4,000 IU daily, along with 1,000 mg calcium carbonate)
- 6ヵ月後、主要評価項目である症状の群間改善はなし
- これらのデータからは現時点ではビタミンD経口補給はAIMSSの予防や治療に適応されない
Switching AI Therapy
-
the Articular Tolerance of Letrozole (ATOLL) study Breast Cancer Res Treat 120:127-134, 2010
-
AIMSSのためにアナストロゾールを中止した女性179名が、1ヶ月の休薬期間を経てレトロゾールの投与を開始した
-
結果、6ヵ月後時点では72%の女性がレトロゾール投与を継続している
-
74%の女性は依然としてAIMSSが存在するが重症度は低く、AIMSSが全くないと報告したのは15%のみであった
-
-
Exemestane and Letrozole Pharmacogenetics (ELPh) trial J Clin Oncol 30:936-942, 2012
-
AIを変更した83人の患者のうち、34人(41%)が筋骨格系の症状のために中止した
-
一方で、32名(39%)が最終フォローアップ時にAI治療を継続することができた
-
-
the Study of Letrozole Extension (SOLE) trial Lancet Oncol 19:127-138, 2018
-
4-6年間のadjuvant endocrine therapy後に寛解した閉経後女性患者
-
レトロゾールの継続投与(5年間)またはレトロゾールの間欠投与(9ヶ月間投与後、1〜4年目は3ヶ月休薬、5年目は継続投与)に無作為に割り付け
-
追跡期間中央値 60 ヵ月後、disease-free survival無病生存率は各群で同程度であった
-
乳癌の観点からは、術後補助化学療法における一時的な治療中断は安全かもしれない
-
患者によってはAI療法を2-4週間ほど一時中断後に、AI療法を再開するアプローチも有益と考えられる
-
【CLINICAL PRACTICE RECOMMENDATIONS】
AIMSSの予防と管理のためのアルゴリズム
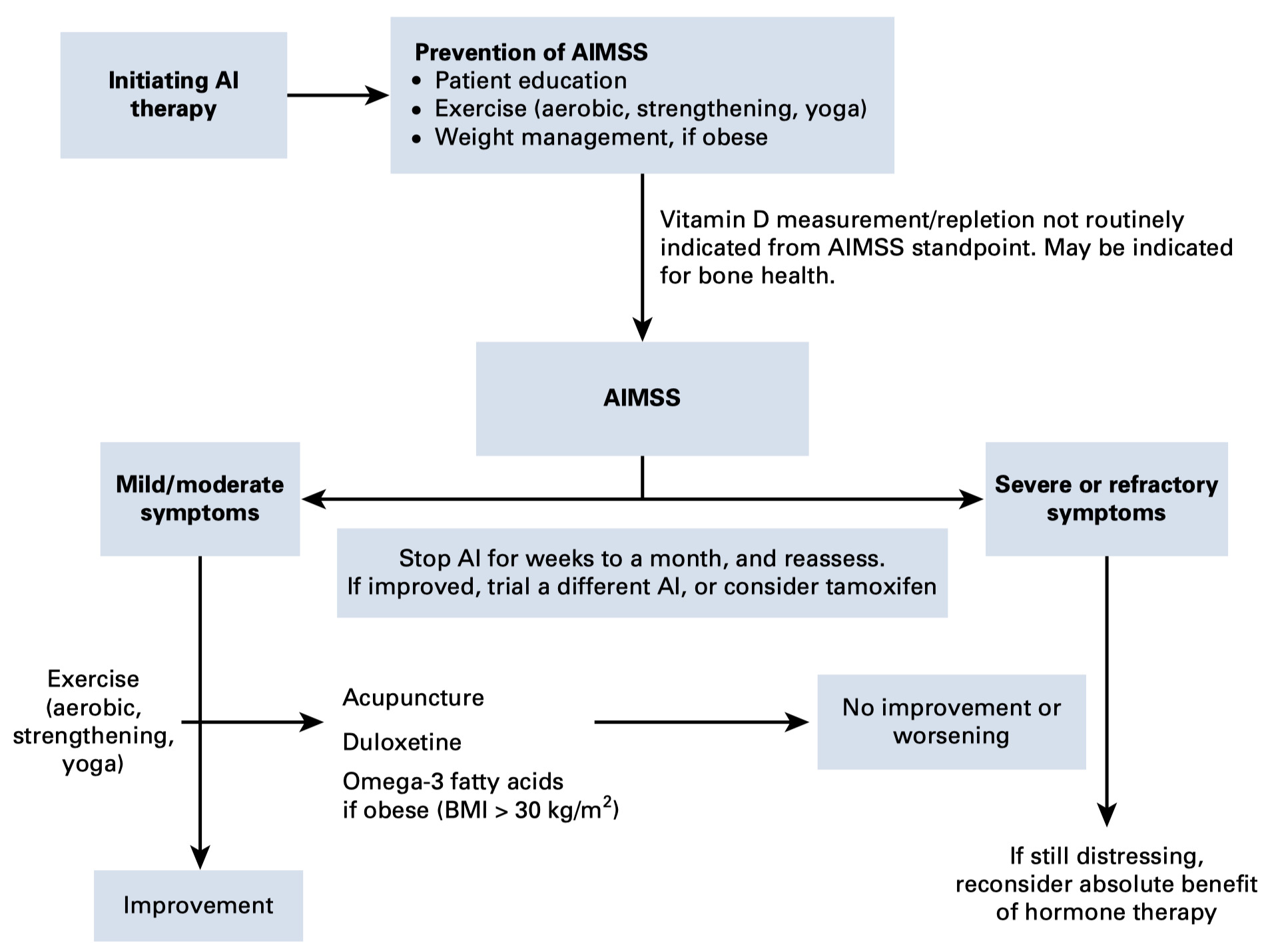
-
ヨガを含む運動はAIMSSの予防・治療に有用であるし、健康そのものにも利点であるため、推奨される
-
ビタミンDはAIMSSの管理では特に必要はない。しかし、骨の健康を含め、他の健康上の利点はある
-
デュロキセチンは不安症、うつ病、慢性変形性関節症の疼痛が共存する患者にはメリットがあるかもしれない
-
肥満の女性にはO3 FAも試してみるのもよさそう
-
ポリファーマシーの制限がある場合は、AI療法を数週間中止してみる
-
乳癌の治療成績の観点から安全でないと懸念する患者や医師がいるが、最近の術後補助療法データでは、AIを9ヶ月投与し,その後3ヶ月休薬することを5年間繰り返しても有用性は低下しない
-
多くの場合、2-4週間の休薬で症状は劇的に軽減する
-
休薬後のAI再投与では初回投与時よりも忍容性が向上する
-
別のアプローチで、AI療法からタモキシフェン療法に切り替える方法もある
-
がんのステージによって異なるかもしれないが、これら2剤併用の乳がん治療効果には大きな差はない
-
タモキシフェンはAIでよく見られるような関節痛を起こさないことが多いが、タモキシフェン投与開始後に関節痛を訴える患者もいる
-
CTSやトリガーフィンガーは改善するのには時間がかかるものの、ほとんどの症状は数週間かけて改善される
-
症状が改善しない場合、もう一度AIMSSの診断を再考し、他の病態が症状の原因となっていないかどうかを検索する
-
リウマチ関連もあるかもしれない。また早期乳癌やマルチな高齢疾患患者は、AIによるベネフィットはほとんど得られないため、内分泌療法を中止することを支持する
(Summary)
- AIMSSはAIの重要でやっかいな毒性であり、これに対するこの重要な治療法のtolerability忍容性を制限する可能性がある
- これらの悪化する症状の予防や治療のために、忍容性があり、利用しやすく、効果的な治療法を見つけるために、さらなる研究が必要である。





