
Differentiating between UCTD and early-stage SLE: from definitions to clinical approach. Nat Rev Rheumatol. 2022 Jan;18(1):9-21.
【Conclusions】
-
臨床の現場では、自己免疫疾患を示唆する臨床的・血清学的特徴を持ちながら、定義されたCTDの診断に至らない患者は少なくない
-
このような患者を定義するために長年使用されてきたnomenclature命名法には一貫性がなく、利用可能な研究の比較可能性も制限がある
-
UCTD, earlystage SLE and definite SLEの臨床症状は疾患経過のある時点において重複している可能性があるが、これらの疾患を区別することは、これらの患者に tailored適したフォローと管理を行うために重要
-
今後の課題は、既存のclassification criteria分類基準を超えて、共通したコンセンサスを作ることである
-
その内容としてはUCTD・early SLEからdefinite CTDへの進行を予測するためのclinical variables臨床変数やdiseasespecific antibody profiles疾患特異的な抗体プロファイルを特定するようなコンセンサスである
-
CTDの分類基準のupdateは、非常に望ましく、UCTD患者における疾患状態の意義のある変化を評価するための、response criteriaを作ることも望ましい。そしてそれは臨床試験や場合によっては臨床現場で使用できるものがよい
-
SLEスペクトラムの疾患については、より具体的な定義を求められており、疾患のサブグループを定義するために分子データを利用すべきである
-
最終的には、将来の目標は、初診時に臨床的に類似している患者を、ベースラインの徴候、症状、血清プロファイルに従ってサブグループに層別化し、オーダーメイドの適した診断・治療経路をデザインするように臨床医の治療に役立つ事である
【Introduction】
-
全身性エリテマトーデス(SLE)は自己免疫疾患であり、免疫調節異常が自己抗体の産生を引き起こし、あらゆる臓器や器官に影響を及ぼしheterogeneousな臨床症状を引き起こす
-
臨床的に定義されたSLEの発症は、数年先までかかることがあり、その理由として免疫異常や臨床症状の発現タイミングをdefinite diagnosis確定診断に必要な閾値を下回るためである J. Autoimmun. 27, 153–160 (2006).
-
実際、初診時にSLEと診断される患者もいるが、SLEを示唆する何らかの症状を呈しながらも確定診断には至らない患者も無視できないほど存在する RMD Open. 4 (Suppl. 1), e000786 (2019).
-
これらの患者さんは以下のどちらかの経過をとる
-
①時間を経るにつれて新しい症状が現れ、SLEと確定診断されるようになるか
-
②何年経ってもSLEを確定診断されるには至らず、病状は限定的で、安定している疾患経過をたどるか
-
-
-
フェーズを表すterm用語があり、latentSLE、intermediateSLE、probableSLE、possibleSLEなどがある。これはdefiniteSLEと診断できない人々の疾患を表すために使われており、その多様な臨床像を定義する試みがなされている
-
しかし、これらの記述的な用語は必ずしもmutually exclusive相互排他的ではなく(それぞれが何らかの定義でがっつり線引きされている訳ではない)、おそらく疾患発症の異なるフェーズで患者さんが混在していることを示している
-
さらに臨床の現場では、自己免疫疾患を示唆するような臨床的・血清学的特徴を認めながら、定義された結合組織病(CTD)に特異的な所見を認めない人が稀ではない
-
これらの人は未分化結合組織病(UCTD)のスペクトラムに入るかもしれない
-
-
UCTDとSLEの初期段階を区別することは難しく、これらの疾患は、SLEを示唆する同様の臨床的特徴を有しているが、確定診断には至らない
(例)UCTDとearly stage SLEを鑑別すること難しい
例えば、抗核抗体、抗SSa/ro抗体、口腔内アフタ症、関節炎が陽性である22歳の女性の症例
CTDに対する特異性の高い徴候や症状がないことから、UCTDの診断が支持される
しかし、治療を行う臨床医がこの患者をimcomlete SLEあるいはearly SLEと考える可能性がある
もし抗二本鎖 DNA 抗体陽性であった場合、診断は SLEに有利に働く
これらの疾患を区別すること重要で、なぜなら徴候や症状の発現から診断までの時間、長期予後が異なることから、フォローアップを計画するに必要だからである
-
関節リウマチ(RA)の研究から、SLEの進化を反映した自然史年表が提案されている Ann. Rheum. Dis. 76, 948–959 (2017).
-
そのようなパラダイムでは、SLEのスペクトルはcontinuumひとつながりに想像することができる
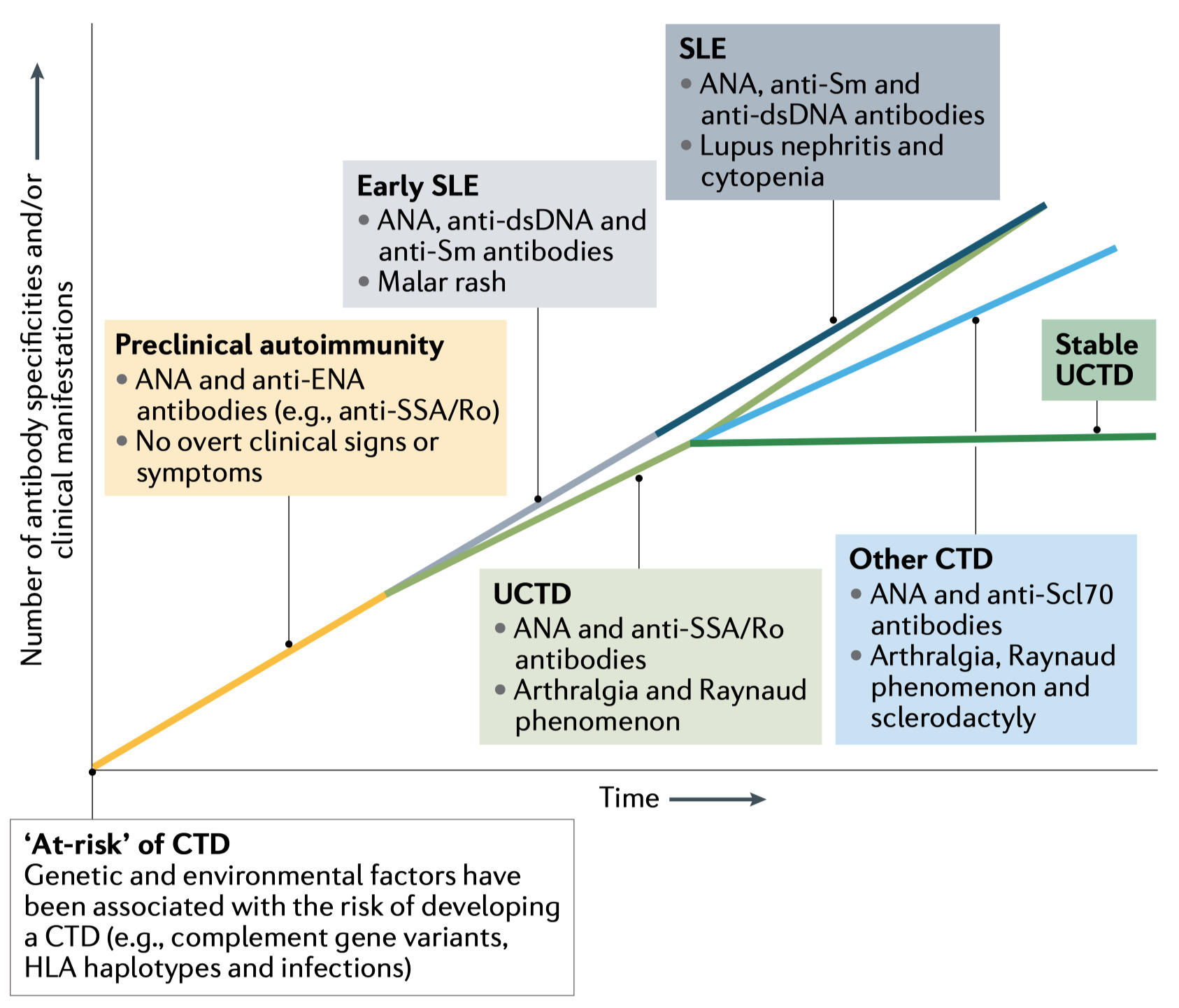
-
SLE発症前、個人はSLEの「危険因子」があり、SLEと関連する遺伝的・環境的リスクファクターは増加している
-
補体遺伝子変異 Nature 582, 577–581 (2020).
-
HLAハプロタイプ Ann. Rheum. Dis. 78, 380–390 (2019).
-
ウイルス感染 Ann. Rheum. Dis. 78, 1235–1241 (2019).
-
-
SLEを発症するリスクの高い人を同定することで、疾病予防のための介入を可能にする可能性がある
-
ひとつながりに考えると、患者の中には無症状の前臨床自己免疫を発症する人もいる(Preclinical autoimmunity)
-
このグループの特徴は、SLEの診断に合致する血清活性を有しており、抗核抗体(ANA)陽性、あるいは抗二本鎖DNA(dsDNA)抗体や抗Sm抗体などのsub血清が陽性であるが、明らかな臨床症状や徴候がない
-
さらに進行すると、血清学的活性を持つ患者は、自己免疫疾患の初期の臨床症状を呈するが、定義されたCTDの診断には至らないパターンとなりうる
-
最終的には、SLEと診断できるような臨床・血清学的症状を伴う本格的な疾患を発症する可能性がある
-
-
このように、病気の自然経過の中では、将来の結果を予測することが困難な段階がある
-
病状が安定したままなのか、それとも本格的なSLEに進展していくのか? SLEのearly stageなのか、UCTDなのか?
本総説の目的
-
UCTDと早期SLEに関する現在の理解、およびSLEの早期発見の可能性についてレビューすること
-
特に、これらの疾患を有する患者をマネジメントする際に臨床的・病原学的に役立つものを考察する
-
妊娠計画を含むUCTDの管理に関する一般的なコメントと、SLEの早期発見と発症による不可逆的な標的臓器障害を防ぐための今後の研究の方向性について述べる
【UCTD or early-stage SLE?】
-
UCTDとは、既存のCTDの診断基準や分類基準のいずれにも当てはまらない臨床症状や免疫学的症状を呈する一連の自己免疫疾患を指す
-
発症時には、(コホート研究では最大50%と)かなりの割合の患者が分類不能の疾患となる可能性がある Best. Pract. Res. Clin. Rheumatol. 21, 1011–1023 (2007).
-
UCTDとSLEを論じる際に留意すべき重要なポイントは、分類と診断が異なるエントリーであること
-
分類基準は、標準化された病態の定義に基づいて作成され、主に臨床研究のための均一な患者群を作るために用いられる
-
長年にわたっていくつかの分類基準が開発されきたが、それは研究者がSLE患者の均一な患者群を特定するためである Ann. Rheum. Dis. 78, 1151–1159 (2019).
-
-
一方で、SLEやUCTDにはdiagnostic criteria診断基準がなく、診断のプロセスは医師の判断によるものであり、徴候や症状がどれくらい集まっているかを認識することによる
-
それゆえに文献に見られるambiguity曖昧さのほとんどが最新の分類基準がないことに起因していますが、臨床の現場では、UCTDとSLEのearly stagesとの区別は、最終的には医師の判断に依存している
-
-
病気の経過中に、UCTD患者の中には以下の疾患を発症する人もいる Autoimmun. Rev. 10, 256–258 (2011).
-
SLE
-
systemic sclerosis (SSc)
-
Sjögren syndrome
-
dermatomyositis
-
polymyositis
-
mixed connective tissue disease
-
RA
-
-
UCTD 患者の症状は以下の通り Rheumatology 59, 2412–2418 (2020).
-
最も一般的な症状は関節炎であり、患者の最大60%に認められる
-
皮膚症状、特に光線過敏症はUCTDと初期のSLEによく認められる
-
しかしながらmalar rash掌蹠膿疱症、discoid rash円板状皮疹、 chronic cutaneous lupu慢性皮膚ループスなどの臨床症状はUCTDよりもSLEの診断を支持するものである
-
白血球減少や血小板減少などの血液疾患も、UCTD患者の約半数に認められる
-
一方、重症SLEの症状である腎疾患、神経病変、溶血性貧血などのはUCTDではまれ
-
-
ここ数年でUCTDに対する理解は進んでおり、 ‘UCTD concept’ が強調されている J. Autoimmun. 48–49, 50–52 (2014).
-
その内容としては、非特異的な特徴を持つ患者を指し示すこと言葉から、本格的なCTDsとは異なる明確な疾患表現型へと分類基準を超えたもの
-
-
様々なUCTDコホートの追跡調査により、UCTD患者の多くはfollowup period追跡期間中に臨床的及・血清学的な異常が後に発生しないことが明らかにされている(stable UCTDとして知られている)
-
stable UCTDの患者数は研究によって異なるが、患者の最大60%になりうる Autoimmun. Rev. 10, 256–258 (2011).
-
stable UCTDは通常、症状が限られており、重度の臓器障害がなく、SLEに比べて陽性となる自己抗体のサブタイプがより少ないことが特徴である
-
-
early or evolving UCTDとは、stable UCTDとは違って、短期間内に明確なCTDにより進展しやすい初期の疾患像を指すが、場合によっては、発症から数年かけて進展することもある Autoimmun. Rev. 10, 256–258 (2011).
-
UCTD全患者のフォローアップにおけるシナリオの中には、手術、ワクチン接種、治療法の変更、併発する感染症など、特別な注意が必要なものもある
-
同様に、妊娠中のカウンセリングとマネジメントにも特別な注意を払う必要があり、母体と胎児の転帰を改善するために集学的なアプローチが必要となる
-
UCTDは妊娠可能な年齢の女性に最も多くみられるリウマチ性疾患の一つ
-
妊婦における未診断のUCTDの有病率は、2.5%に達する可能性があると示唆している論文がある BJOG 115, 51–57 (2008).
-
あるの研究でUCTDを持つ女性は一般集団と比較して、全妊娠の25~30%まで有害な妊娠転帰の有病率が増加すると報告されている BMC Pregnancy Childbirth 16, 313 (2016).
-
重要な点として、UCTD患者においては、妊娠前に抽出性核抗原プロファイリング・抗リン脂質抗体(aPls)が必須
-
母体の抗SSa/ro抗体の存在と関連する新生児皮膚ループスなどの他の合併症を発症する可能性がある Rheumatol. 11, 301–312 (2015).
-
抗リン脂質抗体(aPls)の存在は、子癇前症・早産・子宮内成長制限・子宮内胎児死亡などの不良の妊娠転帰と強く関連している Obstet. Gynecol. 29, 397–403 (2017).
-
-
stable UCTDと定義されたCTDの初期段階を見分けることができれば、治療や予後に影響を与えることができる
-
どの患者が stable UCTDを維持する可能性が最も高いかを特定する際に、臨床・血清の両変数を用いるべきである
-
さらに、‘early’ or ‘incomplete’ SLE は必ずしも良性の疾患ではないことを示す証拠が増えている Arthritis Care Res. https://doi.org/10.1002/ acr.24391 (2020).
-
このような観察は非常に重要であり、医師が患者をタイムリーに特定して、予後の改善につながるストラテジーを早期に実施することにつながる
-
【How many patients are in the grey area?】
-
特定のCTDに分類されない自己免疫の特徴を持つ患者は、臨床の場では比較的よく見られるが、UCTDやearlystageSLEに関する一貫した疫学データは現状乏しい
-
このような確たるエビデンスがないことは、これらの疾患を定義するために世界中で異なる選択基準が用いられてきたという事実によって説明されるかもしれない
-
年齢、性別、民族性、医療アクセス、社会経済的地位、地理的地域、国籍、環境暴露などの要因も、報告されたデータのheterogeneityの説明になるうる
-
-
SLEを示唆する臨床的・検査的特徴を有するが、定義分類には至らない患者を言及するために文献で用いられているnomenclature命名法はheterogeneous異質である
-
したがって、このレビューでは、特定の研究やコホートに言及する際に用いられる命名法は、各研究で用いられたinclusion criteria or definitioに基づくものである
-
しかし、注意すべきこととして利用可能な文献の分析については考える必要がある
-
incomplete SLE, UCTD or earlystage CTDに対して長年にわたって使用されてきた定義について、文献を系統的に検索することは、このNarrative Reviewの範囲外であった
-
したがって、異なる命名法が使用されていても、分析研究に含まれた患者は、実際には類似または重複した特徴を有しているかもしれない
-
利用可能なデータのまとめは下図
comparability比較可能性をより高めるため、類似の inclusion criteriaを用いた研究はグループ化されている
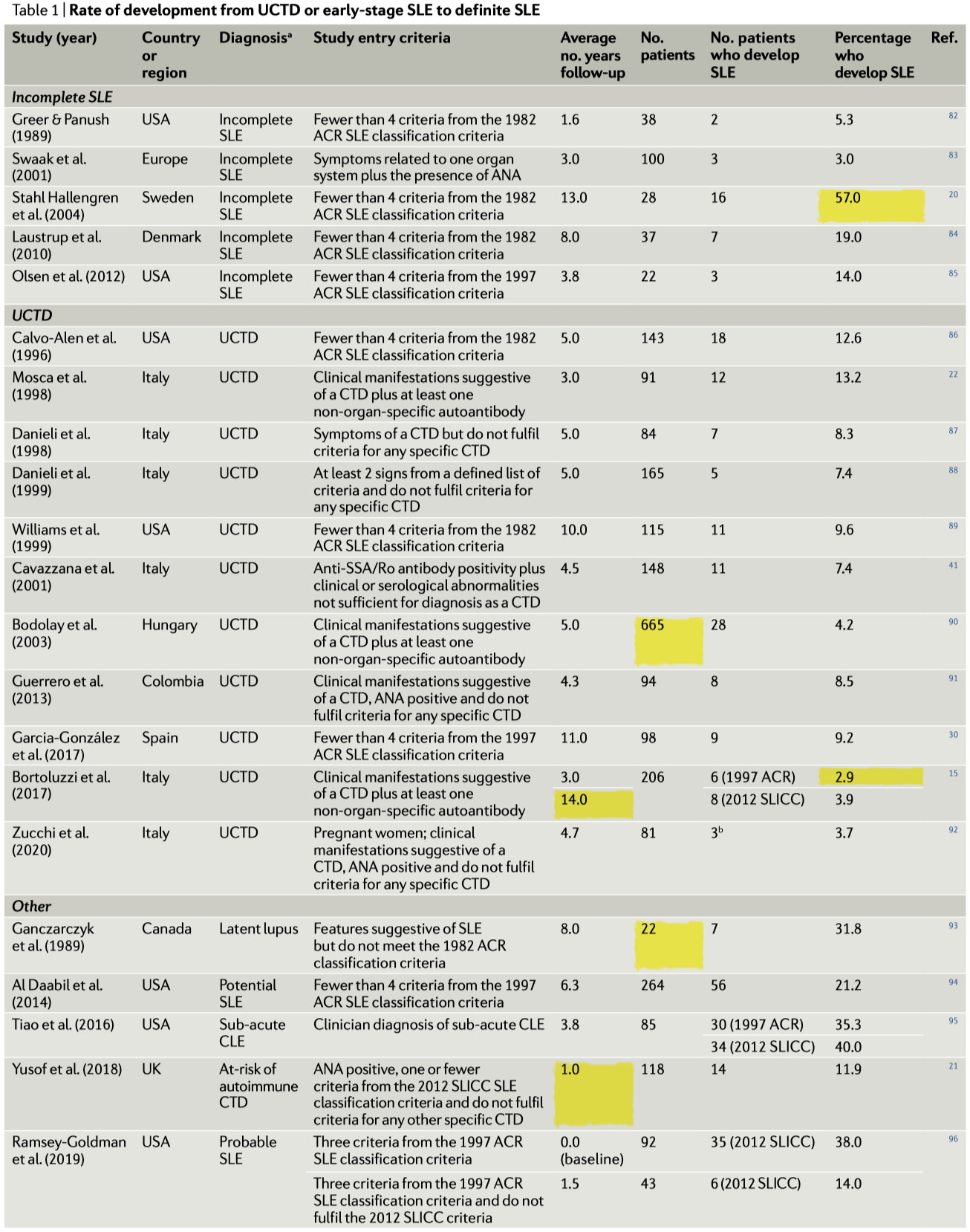
-
SLEへの疾患進行の割合は非常に不均一で、1-3年の期間でその範囲は2.9%から57.0%までであった Ann. Rheum. Dis. 77, 1432–1439 (2018).
-
これらの研究の追跡期間は1年から14年で、登録患者数は22人から665人まで様々
-
イタリアのピサ大学リウマチ科のSinglecentre dataにでは新規紹介患者の20%がCTD(RAを除く)を発症し、そのうちの約13%がUCTDと診断されていた Lupus 7, 95–100 (1998).
(利用可能な疫学的データからわかること)
-
UCTD and earlystage SLEが、リウマチクリニックに通院する患者のかなりの割合を占めるという治療医の認識を支持する
-
しかし、incomplete SLE, earlystage SLE and UCTDの発生率や有病率を正確に推定するには、これらの疾患間の診断上の重複によって、まだ強く制限がある
-
prospective studiesから蓄積された情報では、症状や徴候が現れて、診断されるまでの時間が重要な変数であることは明らかである
-
実際、数年にわたって前向きに追跡調査した患者の経過を比較すると、UCTDの患者は不完全型SLEと診断された患者(範囲3.0~57.0%)と比較して、CTDへの年次進行率が低い(Table 1に含まれる研究では範囲2.9~13.2%)
-
この観察は、UCTDと早期SLEの臨床的区別をよりに支持するものである
-
臨床的な観点から、3年以上にわたって新たな臨床症状や検査所見がなく、CTDに特異的な血清プロファイル(抗DNA抗体や抗Sm抗体など)がないことが、UCTDの診断の根拠となりうる)
-
-
UCTD患者の発症年齢と診断年齢については、RELESSERレジストリのデータで調査されている Medicine 94, e267 (2015).
-
最初の症状:UCTD患者は、確定診断されたSLE患者よりもより高齢(41.0歳対32.6歳)
-
最初の診断:UCTD患者は一般的により高齢でした(42.9歳対34.6歳)
-
ゆえに、UCTDとearlystageSLEを鑑別する際には、症状発現時の年齢を考慮する必要がある
-
-
the Lupus Family Registry and Repository での研究 Rheumatology 50, 47–59 (2011).
-
対照患者について
-
1997 年 ACR SLE 分類基準を満たす患者 3,397 名 Arthritis Rheum. 25, 1271–1277 (1982).
-
この研究の著者がincomplete SLEと定義した患者 291 名(ACR 基準を 3 つ満たし、2012 年 Systemic Lupus International Collaborating Clinics (SLICC) 基準を満たさない患者) Arthritis Rheum. 64, 2677–2686 (2012).
-
-
結果について
-
性差: Lupus Sci. Med. 4, e000176 (2017).
-
どちらの患者群も主に女性(90%近く)であった
-
しかしincomplete SLEは療法の基準を満たしてSLE患者に比べて診断時の年齢が平均的に高かった(47.5歳対42.0歳)
-
-
人種差: Lupus Sci. Med. 4, e000176 (2017).
-
African American:incomplete SLE患者<SLE患者 (23.7% versus 32.6%)
-
Latin American:incomplete SLE患者<SLE ( 4.1% versus 7.2%)
-
European American :incomplete SLE患者>SLE (56.7% versus 44.3%)
-
-
-
【The role of clinical manifestations】
-
earlystage SLE, incomplete SLE and UCTD疑い患者の臨床・検査的特徴はこれらの疾患が最初に診断されたときには、オーバーラップしている可能性がある
-
全体として、UCTD患者は、incomplete SLE患者よりも病状が軽い
-
Peking Union Medical College Hospital Registryではincomplete SLE患者のほぼ1/3は疾患活動性が中程度から高度であった Clin. Rheumatol. 34, 1383–1389 (2015).
-
-
SLICC-ACR Damage Indexによると、incomplete SLE患者の半数以上が臓器障害を認めおり、いくつかの臨床症状は、incomplete SLE患者の方がUCTD患者よりも頻繁に観察された
-
-
肺領域はSLICC-ACR Damage Indexの最も多い領域で22.1%の患者
-
腎領域が11.7%の患者
-
神経領域が10.4%の患者
-
-
-
高血圧・心血管イベント・重症感染症はincomplete SLE患者では、definite SLE患者少ない Lupus Sci. Med. 4, e000176 (2017).
-
-
これらの結果は、RELESSERレジストリでSLE患者に比べてincomplete SLE 患者で入院や死亡の割合が低いことと一致する Medicine 94, e267 (2015).
-
UCTDからdefinite CTD,への移行率を報告した研究を分析する場合はいくつかの検討事項に注目する必要
-
第一に、研究の中には抗DNA抗体陽性や皮疹などSLEに特異的な所見を有する患者をUCTDとして登録する研究がある
-
第二に、UCTDの概念は比較的最近のもので、古い研究が発表された当時はまだ完全には解明されていなかったこと
-
さらに、医療へのアクセスなどの社会疫学的要因が、CTDの進行や予後に影響を与える可能性がある
-
例えば、UK Clinical Practice Research Datalinkのデータでは、SLEと診断される前の5年間で、SLE患者の年間一般医受診率の中央値は9.2であるのに対して、SLEではないとされた患者では3.8であった Arthritis Care Res. 69, 833–841 (2017).
-
したがって、バイアスの一部はリウマチ診療所へのアクセスの不均質さによっても説明できるかもしれない
-
-
-
様々なコホートでそれぞれ対照的な結果が報告されているが、疾患の進行が懸念される場合、治療医に役立つdefiniteCTDsへの進行に関するいくつかの予後因子を特定することができる
-
これらの要因のうち、臨床症状の種類と時期については、いくらかの考慮が必要
-
臨床症状
-
自己免疫性CTDの発症リスクがある患者(ANA陽性、SLICC臨床基準1項目以下、症状期間12ヶ月未満と定義)の前向き研究では、ベースラインで超音波で検出できる滑膜炎が存在する患者は、そうでない患者よりも自己免疫性CTDに進行した患者に多く見られた Ann. Rheum. Dis. 77, 1432–1439 (2018).
-
実際、いくつかの症状(puffy fingers, Gottron’s papules, antiSm antibodies and nephritis)は、definite CTDを示唆するものであり、UCTDの診断を否定する
-
-
症状発現のタイミング
-
CTDへ進行したUCTD患者のうち、最も頻繁に報告されている診断はSLEである(20~60%) Lupus 30, 280–284 (2021).
-
この進行は、最初の臨床症状が現れてから5年以内に起こることが多いが、それ以降に進行する場合もある Arthritis Rheumatol. 71, 91–98 (2019).
-
-
さらに、最終的にSLEを発症した患者は、数カ月から数年の間に臨床症状を認める
-
3つ以上のBritish Isles Lupus Assessment Group index domainsで症状が見られる患者の割合は、診断前の5年間で 18.7% 、SLEと診断される前の1年間で 39.7% に増加した Arthritis Rheumatol. 71, 91–98 (2019).
-
-
-
このレビューではUCTDの新たな分類基準を提示することを目的とはしないが、医師サポートのための留意点がある
-
第一に、definite CTDsの特異度が低いため、いくつかの症状や徴候(例えば、isolated xerostomia or xerophthalmia)は、ANA検査が陽性であっても、UCTDの臨床診断を支持するのに十分でない場合がある
-
この提案は、sicca syndromeシッカ症候群が明確な自己免疫の実体を表していないかもしれないという事実と一致する Clin. Exp. Med. https://doi.org/10.1007/S10238-021-00728-6 (2021).
-
-
第二に、2015年に欧州呼吸器学会と米国胸部学会の合同タスクフォースが、definiteCTDを伴わない、間質性肺疾患と自己免疫の特徴を認める患者の同定を改善するために、interstitial pneumonia with autoimmune features自己免疫の特徴を有する間質性肺炎、という新しい病名の一連の分類基準を提案した Biomedicines 9, 17 (2020).
-
CTDassociated interstitial lung diseaseCTD関連間質性肺疾患(自己免疫機能を有する間質性肺炎を含む)は、一般に予後が良好であり、治療法も両者で大きく異なるため、idiopathic pulmonary fibrosis特発性肺線維症との鑑別は非常に重要である
-
-
全体的に、SLEの確定診断は腎臓、神経系、循環器系の病変を含む臨床症状を呈する患者に対して適用されるべきだが、臨床症状ただ一つからUCTDとearlystage SLEを鑑別することは難しい
-
【The role of the laboratory and autoantibody testing】
-
CTD の診断における主な困難さの一つとして、特徴的な血清学的異常(ANA やリウマトイド因子など)がいくつかの疾患に共通していることがある
-
しかし、抗体の特異性の中には、defined CTD に対する特異性の点から診断的価値を有するものも存在する
-
limited cutaneous SSc に対するanticentromere antibodies抗セントロメア抗体
-
diffuse cutaneous SScに対するantitopoisomeraseI antibodies抗トポイソメラーゼ I 抗体 RMD Open. 4 (Suppl. 1), e000786 (2019).
-
SLE に対する抗 Sm 抗体や抗 DNA 抗体など Expert Rev. Clin. Immunol. 3, 721–738 (2007).
-
-
同様に、患者から検出される抗体特異性のタイプに加えて、検査で陽性となる自己抗体の累積数は、SLEの確定診断に向けた進行の指標となりうる N. Engl. J. Med. 349, 1526–1533 (2003).
-
実際、SLEの患者は1年に平均0.3個の新しい自己抗体特異性を獲得して、診断時には平均3個の自己抗体特異性に対して陽性となる J. Autoimmun. 74, 182–193 (2016).
-
しかしながら、CTD疑い患者を同定するための有意義な前臨床バイオマーカーを同定する必要性が残されている J. Rheumatol. 42, 152–154 (2015).
-
-
抗SS-A/Ro抗体陽性のUCTD患者148人を含む研究では、24%が4.5年以内に、主にSLEや原発性シェーグレン症候群など、定義されたCTDを発症していた Clin. Exp. Rheumatol. 19, 403–409 (2001).
-
UCTD 患者 70 名を対象とした別の研究では、60kDa 抗原を認識する抗SSA/Ro 抗体のみを持つ患者は SLE に移行しやすく、52kDa 抗原を認識する抗SSA/Ro 抗体と60kDa 抗原を認識する抗体の両方を持つ患者は、原発性シェーグレン症候群に移行しやすかった Jt. Bone Spine 67, 183–187 (2000).
-
この知見に基づいて、Ro52+ Ro60- 患者97人とRo52+ Ro60+患者100人を含むレトロスペクティブ研究 J. Clin. Pathol. 71, 12–19 (2018).
-
Ro52+ Ro60 -患者の70%以上はCTDと診断され、その内訳は以下の通り
-
UCTD(14%)
-
RA(13%)
-
SLE(10%)
-
Sjögren syndrome(10%)
-
-
Ro52+ Ro60-の23人(24%)はCTDと診断されなかった Nature 582, 577–581 (2020).
-
Ro52+ Ro60 +患者の87%はCTDと診断され、その内訳は以下の通り
-
Sjögren syndrome(34%)
-
SLE(23%)
-
UCTD(12%)
-
-
-
earlystage UCTDの症状を少なくとも1年以上示した患者213人を対象としたUSAの研究 で、5年後のSLE発症は、以下と関連性があった J. Rheumatol. 18, 1332–1339 (1991).
-
-
特定の人口統計学的特徴(アフリカ系アメリカ人、若年)
-
臨床症状(pleuritis胸膜炎やpericarditis心膜炎、alopecia脱毛症、discoid lesions円板状病変)
-
検査値異常(homogeneous ANAパターン、抗DNA抗体や抗Sm抗体、クームス試験陽性、梅毒偽陽性falsepositive)
-
検査項目のうち、SLEと最も強い関連を示したのは、homogeneous ANA patternと抗Sm抗体
-
-
-
-
130人のSLE患者を対象とした研究 Arthritis Rheum. 50, 1226–1232 (2004).
-
18.5%の患者がSLEと確定診断される前にIgGまたはIgM抗カルジオリピン(aCL)抗体が陽性となった
-
aCL抗体はSLE発症の最大7.6年前まで((平均3年)に検出できることが証明された
-
aCL抗体陽性は予後不良と関連あり
-
神経系、腎系、血液系の合併症の有病率が高く、血栓イベントのリスクも高い
-
-
-
自己抗体は、CTDの分類プロセスの一部であるだけでなく、合併症や併存疾患を予測するためのバイオマーカーとして重要な役割を担っている
-
臨床現場では、患者は特定のCTDに特異的ではないけれども、ANA陽性を示すことは多く、抽出可能な核内抗原プロファイリングを行わないため、疾患経過の予測可能性には限りがある
-
自己抗体の特異性に基づいて、重篤な疾患症状や臓器障害を発症するリスクの高いUCTD患者を特定できれば、医師はこれらの患者に合わせたマネジメントおよびフォローアップを計画することが可能となる
-
自己抗体プロファイリングは、以前にUCTDに診断されている患者の管理指針として特に重要である
-
追加の特異的自己抗体を検出することで、疾患の進行の可能性を高めるだけでなく、調査や治療への迅速なアプローチにつながることになる Neuropathol. Appl. Neurobiol. 43, 62–81 (2017).
-
例えば、抗DNA抗体や抗Sm抗体が検出されたUCTD患者では、腎機能の精査や尿検査を実施すべき
-
SScを示唆する自己抗体プロファイルが検出されたUCTD患者では、心肺機能検査や悪性腫瘍スクリーニングを実施すべき
-
-
【The role of classification criteria】
-
過去数年間で、CTDsの迅速な診断と分類を促進する証拠が増え、多くの疾患について新しい分類基準が開発された
-
2010年には、RAのearly stagesを捉える試みとして、RAの新しい分類基準が発表された Ann. Rheum. Dis. 69, 1580–1588 (2010).
-
新しい基準を適用した場合、1987年のACRのRA分類基準を用いた推定値と比較して、undifferentiated arthritis 未分化関節炎の有病率が減少したことが研究により示されている Ann. Rheum. Dis. 72, 1335–1341 (2013).
-
-
レイノー現象、指の腫れ、ANA検査陽性という3つのレッドフラッグが確認され、SScのvery early診断へのステップもなされた Ann. Rheum. Dis. 70, 476–481 (2011).
-
SLEにおいても、early classification早期分類の重要性が出てきた
-
-
2012年のSLEに対するSLICCの分類基準は、1997年版ACRのSLE分類基準よりも臨床的に有効となるように設計されている
-
それによりACR基準を用いた場合よりも多くの臨床的なdefined SLE患者を研究対象に含めることが可能となった Arthritis Rheum. 64, 2677–2686 (2012).
-
現在の分類基準のいずれもUCTD と SLE (early or definite)を区別するためのトピックに対応するようには設計されていない
-
しかし、1997年のACR基準と2012年のSLICC基準の正確性は、世界中の特定のコホートのUCTD患者で検証されている
-
研究数は限られており、デザインおよびinclusion criteriaが異なる研究間でデータを比較する可能性に影響するが、いくつかの知見は注目に値する
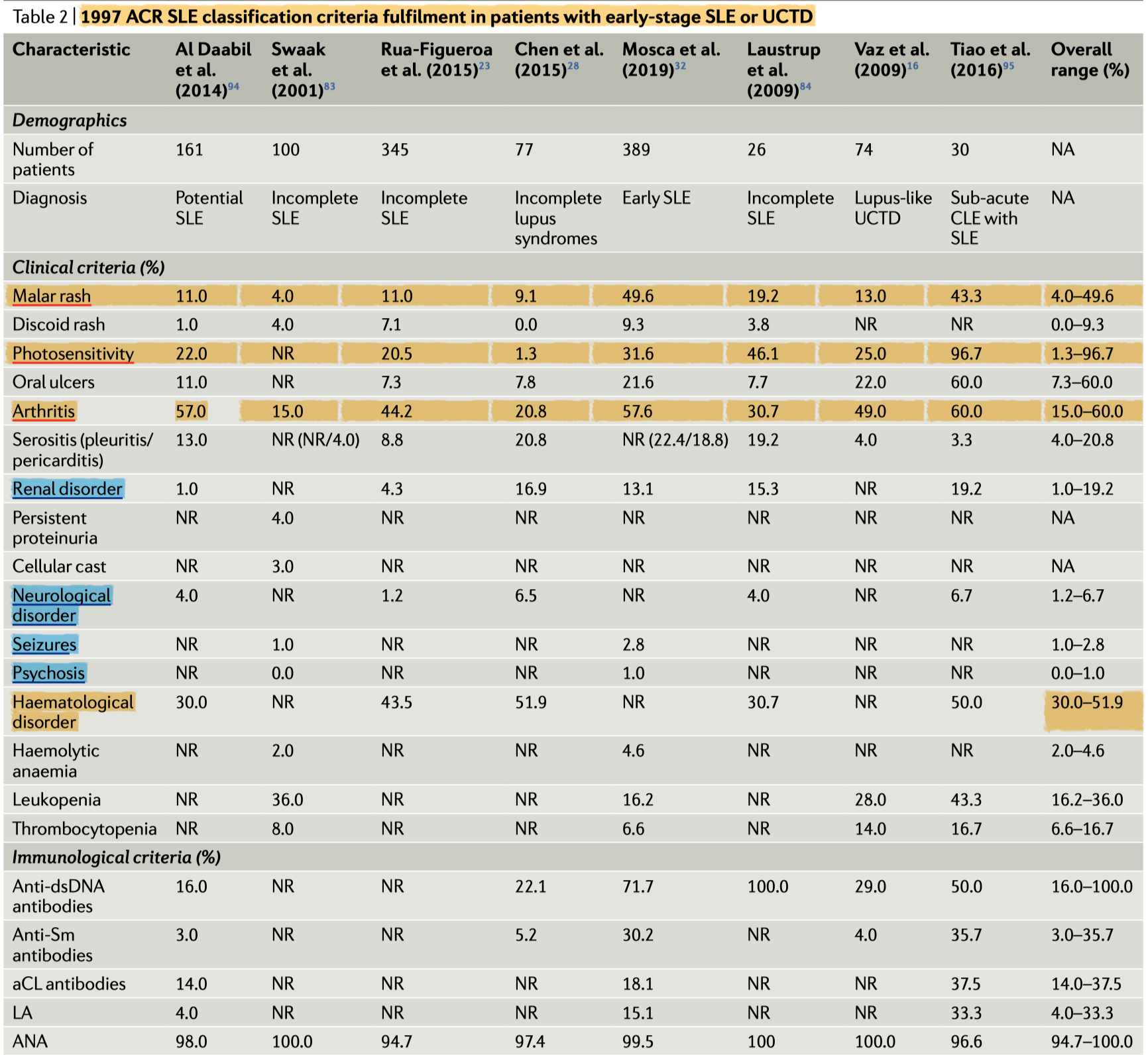
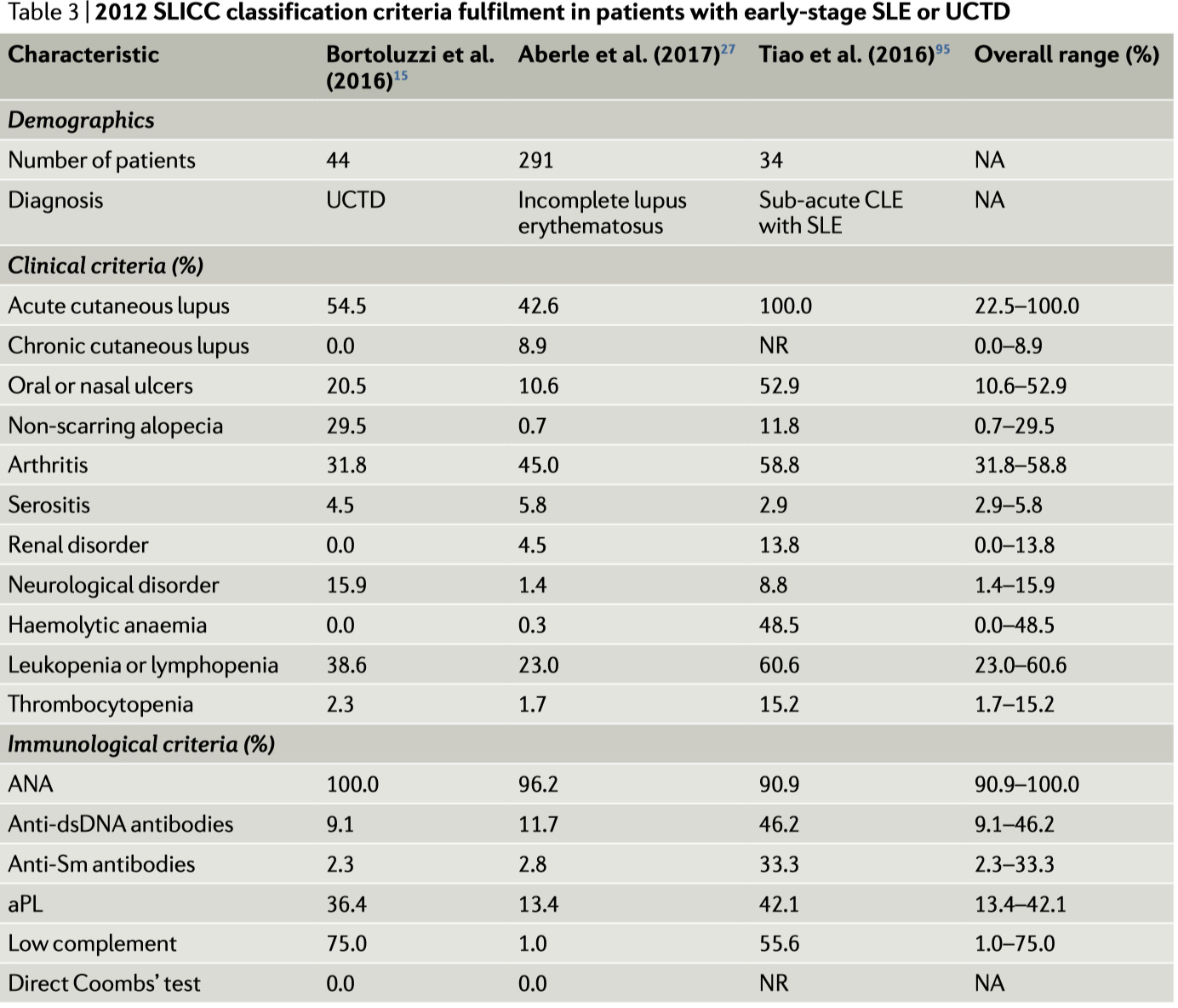
-
incomplete SLEやUCTDの患者で報告されている1997年のACRと2012年のSLICCの分類基準セットでは、臨床症状は皮膚と関節への影響が最も多い
-
一方で、腎臓と中枢神経への影響はあまり報告されていない
-
これらの後者の所見は驚くべきものではない。なぜなら皮膚や関節の症状よりもdefinite SLEと診断される可能性が高いからである
-
興味深いことに、血液疾患(特に白血球減少やリンパ球減少)はよくみられるが、thrombocytopenia血小板減少はこれらの患者では比較的少ない
-
1997年のACR、2012年のSLICCの分類基準を用いた研究を比較しても、大きな違いはない
-
しかし、1997年ACR分類基準でも2012年のSLICC分類基準でもSLEに分類されなかったUCTDの女性133人のコホートでは、2019年EULAR-ACR分類基準を適用すると、17%がSLEと分類された Arthritis Care Res. https://doi.org/10.1002/ acr.24391 (2020).
-
これらの観察から、分類基準は研究目的では必要だが、臨床では抗DNA抗体、抗Sm抗体、malar rashといった特徴が確認されれば、SLE有利へと診断に影響する
-
検査の観点からは、抗DNA抗体陽性が1997年のACR基準(Table 2)を用いた研究では最大100%の患者で、2012年のSLICC基準(Table 3)を用いた研究では最大46%の患者で報告された
-
この点は重要である
-
抗DNA抗体陽性と判定された患者さんがUCTDであると言えるのか?
-
あるいは、抗DNA抗体の存在は、UCTDの診断をルールアウトして、earlystage SLE or SLEの診断に有利にすべきなのか?
-
SLEに対する抗DNA抗体や抗Sm抗体の特異性は疑わないが、現在のところ、診断の判断は純粋に臨床的な判断に依存している
-
SLEに特異的な症状があればdefinite CTDと診断される可能性があるため、fullblown本格的なSLEとearlystage SLEを区別するには、臨床症状および徴候・症状の発現と診断までの時期の両方に依存する必要があるだろう
-
-
-
全体として、UCTDに関しては、研究によっていくらか違いはあるものの、利用可能な文献では以下の定義に収束しているようである
-
CTDを示唆する徴候・症状があるが定義されたCTDの基準を満たさないこと、
-
ANA検査が陽性であること、
-
疾患期間が1年以上であること
-
-
incomplete SLE患者を含む研究は通常、SLEのACR基準項目を4つ未満しか満たしていない患者のことを述べている
-
early SLEの定義は最も heterogeneousで、確固たるコンセンサスはまだ存在してない
-
この定義を用いた研究は、通常、経験豊富なリウマチ専門医が臨床経験と判断に基づいて下した診断に言及している Arthritis Rheumatol. 71, 91–98 (2019).
-
現在の課題は、research studiesで使用された定義を臨床に反映させることである
-
そこで、著者等はSLEスペクトラム障害とUCTDの好ましい命名法をで紹介する
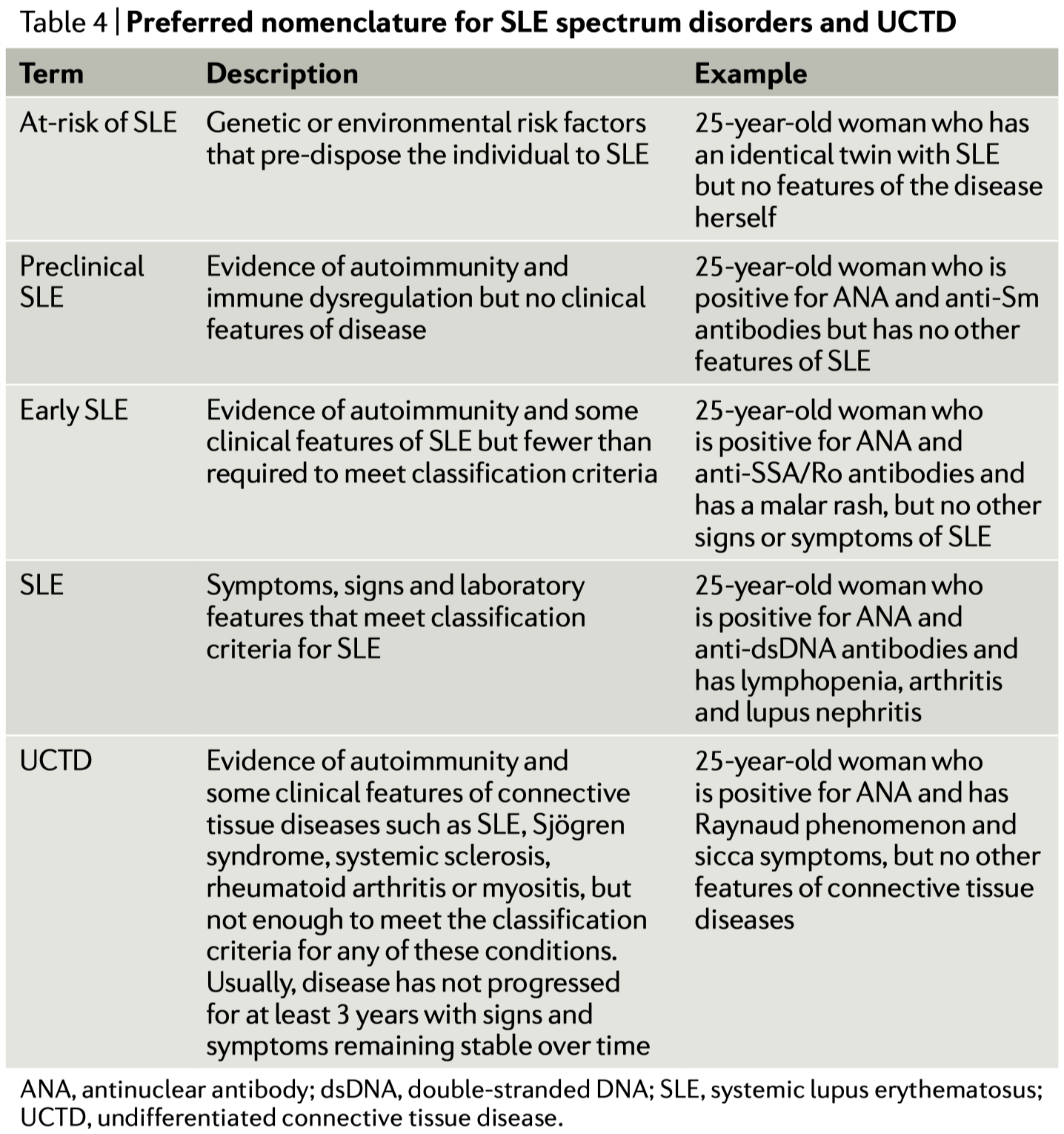
【Can we prevent progression to SLE?】
-
UCTDを発症した患者がその後どのくらいの期間でSLEを発症するかはまだ解明されていない
-
しかし、これまでのセクションで述べたデータに基づくと、SLEに進行するリスクのある患者を特定することは可能である
-
同様に、どのような治療的介入をすれば、確定的なリウマチ性疾患の発症を予防・遅延させることができるのかどうかについても、十分には分かっていない
-
そのため、CTDに分類できない疾患を持つ患者のマネジメントは、患者の臨床症状に応じて個別に調整され、舵を取る必要がある
-
例えば、SLEを示唆する特徴を有する患者は、腎病変のような生命を脅かす徴候をできるだけ早期に発見できるように、臨床検査とともに定期的に血液検査や尿検査を行い密に観察する必要がある
-
一方で、SScを示唆する徴候や自己抗体プロファイルを持つ患者のサーベイランスには、PAHを発症するリスクが高いため、心エコー検査を含める必要がある Autoimmu. Rev. 16, 796–802 (2017).
-
UCTDのマネジメント戦略に関するRCTは明確な分類基準がないため、これまで実施されたことはない
-
このため、UCTD患者の治療マネジメントはは主に治療ガイドラインや、SLE・RA・SSc・myositisのような定義されたリウマチ性疾患の患者にもみられる症状(関節炎や皮膚症状など)に対する治療ガイドラインや対症療法によるところが現状である
-
早期治療の主な目的は、治療の遅れに関連する長期的な合併症を減らすことであり、最終的な目標は不可逆的な臓器障害と死亡率を最小化にすること
-
9,000人以上のSLE患者を対象とした調査では、臨床症状が現れてから6ヵ月以内に診断された患者は、6ヵ月以降に診断された患者に比べて、フレアがより少なく、入院率やSLE関連の総費用がより少なかったという結果が出ている Appl. Health Econ. Health Policy 12, 179–190 (2014).
-
これらの結果は、診断が早ければ早いほど、疾病関連被害に関してより大きな利益をもたらす可能性があることを示唆している
-
現在、earlystage SLE患者を対象としたいくつかの研究活動が進行中である ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03804723 (2019).
-
現在までに、preclinical SLE患者の管理における一次予防に関するコンセンサスは得られていない(preclinical SLE: 自己免疫や免疫異常の証拠はあるが、この疾患の臨床的特徴はない患者)
-
このようにコンセンサスが欠如している理由は、無症状のANA陽性者に対する治療が、臨床的に関連するCTDの発症を防ぐことができるという考えを支持するには限定的なエビデンスしかないからである
-
US military米軍兵士を対象としたretrospective studyで診断前の抗マラリア薬ヒドロキシクロロキンの使用がSLEの発症遅延と関連していることが報告された Lupus 16, 401–409 (2007).
-
1997年のACRのSLE分類基準を満たした130人のうち、診断前にヒドロキシクロロキンを使用していた人は、使用していなかった人に比べ、最初の臨床症状の発症からSLE分類までの時間が長かった(1.08年対0.29年)
-
-
これらの結果は有望であるように思えるが、他の薬剤の様に、抗マラリア薬にも有害事象があることを留意する必要がある
-
したがって、無症状患者における一次予防として抗マラリア薬の使用を検討する際には、リスクとベネフィットのバランスを慎重に評価することが必要で、このsettingでの使用を支持する確固たる証拠はまだない Appl. Health Econ. Health Policy 12, 179–190 (2014).
-
UCTDやearlystage SLE患者において、最終的にdefinite SLEの発症に関与する可能性は除外できないが、ヒドロキシクロロキンの使用は臨床判断に基づき、一次予防としてではなく、進行中の臨床症状のコントロールを試みるためときに限って使用する必要がある
-
しかし、現在動物モデルでSLE発症を抑制するために、様々な免疫調節や免疫抑制の役割を検討するエビデンスが増えつつある J. Immunol. 203, 58–75 (2019).
-
今後の課題は2つ
-
一つはSLEのリスクのある患者に対して、発症を回避するためのストラテジーを作成する必要がある
-
トリガー因子
-
現実的な観点からは、ANAが持続的に単独で陽性である無症状の患者さんに対しては、誘因となりうるトリガー因子(喫煙、SLEを誘発する薬剤、過度の太陽光照射など)を取り除く目的で、注意深い監視と適切なカウンセリングを行うことが妥当な方法
-
-
ビタミンDは議論中
-
definite CTDへの進展リスクを軽減するためのビタミンDの潜在的な免疫調節的な役割については議論の余地がある J. Autoimmun. 74, 73–84 (2016).
-
現時点では、systemic autoimmune diseases全身性自己免疫疾患を発症するリスクのある人にビタミンD補給を系統的に行うことを支持する確かなエビデンスは得られていない
-
-
HCQ
-
SLEに関連した自己抗体(抗DNA抗体、抗Sm抗体、抗SS-A/Ro抗体、抗SS-B/La抗体)や補体の減少(C3、C4濃度が低い)を伴う無症状のANA陽性者では、疾患進行のリスクを減らすためにヒドロキシクロロキンの投与が合理的に考えられる Autoimmun. Rev. 10, 55–60 (2010).
-
-
-
一方で、SLE患者さんに対する信頼できるプロファイリングのアプローチを作成する必要がある、それは、ループス腎炎のような特定臓器病変を発症するリスクの高い患者さんを特定し、それに応じて管理手法を調整できるようにするためである
-
-
その他
-
他の自己抗体の特異性が陽性であることは、一次予防の可能性を示すかもしれない
-
例えば、抗リン脂質抗体(aPL)の無症状キャリアにおいて、特に血栓症のリスクが高いプロファイル(複数のaPL特異性や高い力価など)が検出された場合、血栓症のリスクが高まる Thromb. Hemost. 38, 322–327 (2012).
-
しかし、抗血栓療法の慢性使用に伴う本質的な出血のリスクも評価されるべき
-
同様に、無症状の aPLキャリアでは、時限的な抗血栓予防法(低分子ヘパリンなど)は、血栓を誘発する可能性のある要因(手術や長 期間の固定化など)との関連で評価でき、担当臨床医が慎重に評価・管理する必要がある
-
【Future directions】
Advancing diagnosis
-
UCTD, preclinical SLE and earlystage SLEのセッティングにおける診断精度を向上させるために、いくつかの要素を考慮する必要がある
-
第一に、CTDのvery early stagesおよびUCTDからCTDへの進行に関して、両方の基礎にあるにある発症メカニズムを解明すること
-
健康なボランティアを含む大規模な初期段階のearlystage CTDとUCTDコホートの縦断的研究と多項目解析プラットフォームのような新しい技術が、疾患がどのように進行するかをより理解するのに必要とされている
-
これらの新しいmultianalyte omics technologiesは、医師が疾患経過全体を通して起こる発症プロセスを理解するのに役立つ、新しいバイオマーカーを提供する可能性がある65
-
このような技術は、現在のトライアンドエラーに頼ったものから、患者層別化システムをより正確なものへとシフトし、新しい臨床試験やエビデンスに基づいた個別化治療の設計を導く可能性がある Arthritis Rheumatol. 69, 487–493 (2017).
-
-
診断を向上させるためにはいくつかの技術的な問題にも対処する必要がある
-
自己抗体プロファイリングの標準化されたフォローアップ検査アルゴリズムの開発など
-
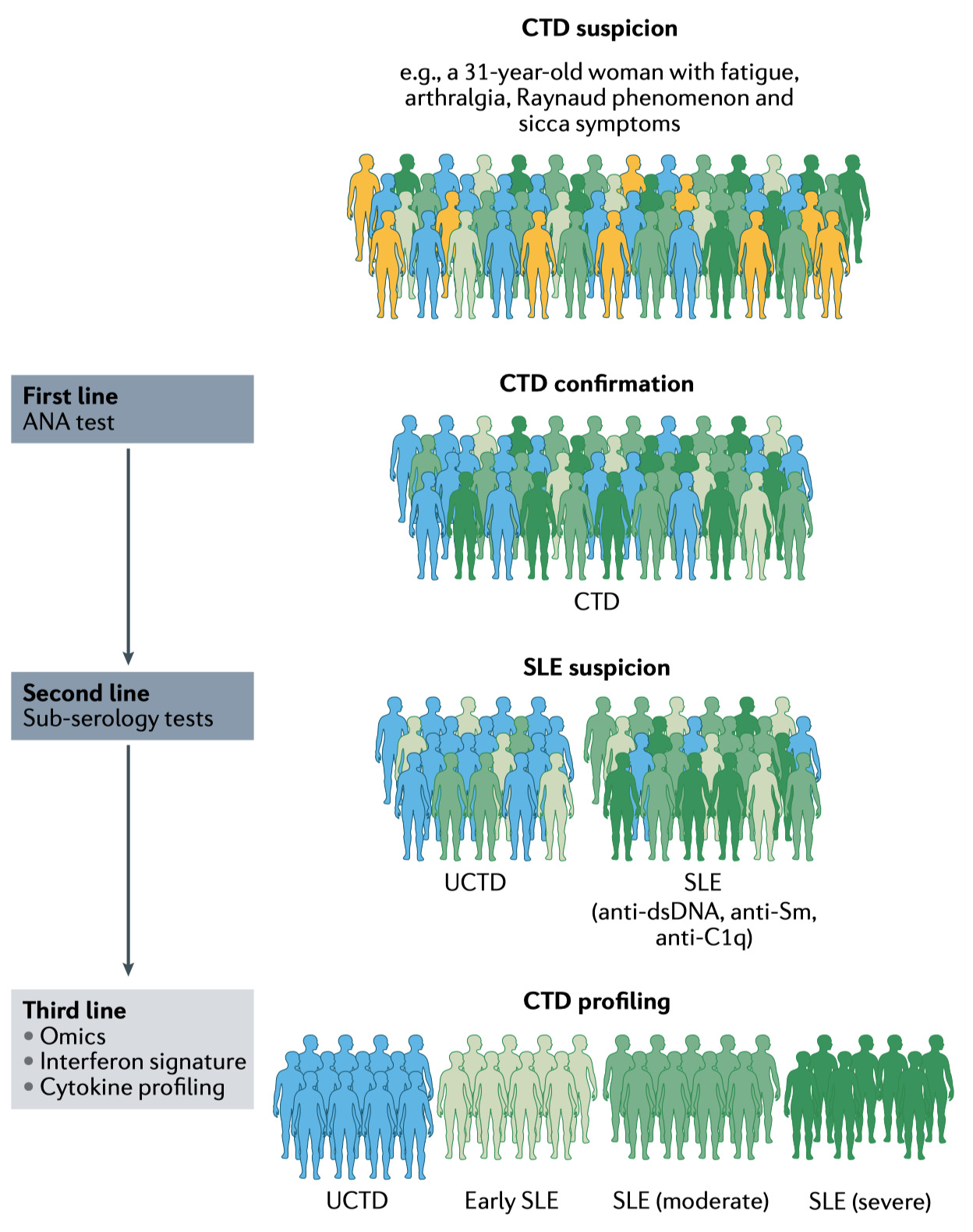
The ANA indirect immunofluorescence testANA間接免疫蛍光法検査には、現在、UCTD・SLE・その他のCTDのスクリーニング検査として選択されている
-
しかし、将来的には、多項目固相アッセイを用いることで追跡検査アルゴリズムが行えるようになり、疾患固有のターゲットを認識する自己抗体を効率的かつ経済的に検出できる可能性がある Lancet 392, 1330–1339 (2018).
-
-
従来の考え方では、たとえ1つの自己抗体(ANAなど)が陽性であっても、診断の示唆には十分であるという概念を支持してきた
-
しかし、今 後は、各自己抗体が疾患の層別化や治療・予後に対するエビデンスに基づくアプローチのための付加価値を提供し、また正確な診断のための価値を提供できるという仮説を支持するようなパラダイムシフトが必要である
-
-
自己抗体検査の特異度、感度、予測値の観点から、CTDの診断精度は、多項目分析プラットフォームへの人工知能技術の適用、すなわちアルゴリズム解析を伴う多項目分析アレイとして言及されるパラダイムシフトによって向上すると予想される Cell 165, 551–565 (2016).
-
診断的アプローチの課題は、特定の治療薬からベネフィットを得るベストチャンスを有する可患者を特定することである Ann. Transl. Med. 4, 482 (2016).
-
この目標に向けて、自己免疫疾患の基礎にある分子経路の理解を解明していくことが、バイオマーカーの同定につながり、CTD患者を同定し、最終的に新規の治療法選択へガイドすることになる Nat. Rev. Rheumatol. 14, 354–362 (2018).
炎症性サイトカインプロファイル
-
炎症性サイトカインプロファイルの初期変化は、長い時間をかけて臨床症状の発現に先行する Ann. Rheum. Dis. 75, 2014–2021 (2016).
-
例えば、IFNγ濃度の上昇は、SLEの診断に3年以上先行することがある Cytokine 146, 155633 (2021).
-
-
IFNは自然・適応免疫系の両方に多くの影響を及ぼし、自己免疫におけるその役割の重要性が徐々に理解されつつある
-
IFNはantigenpresenting cells抗原提示細胞からplasmacytoid dendritic cells形質細胞様樹状細胞、B細胞、T細胞まで、あらゆるレベルで免疫反応に影響を与える可能性がある
-
その上、IFNγはインターフェロンの抗RNA抗体産生のトリガーとなり、I型インターフェロンの増加とそれに続くカスケードを引き起こす原因となりうる Cytokine 146, 155633 (2021).
-
ANA 陽性者 57 名を、年齢的にマッチした健常者、SLE 患者と比較した研究では、炎症性サイトカイン(IL17、TNF、IFNγ など)の発現量がstepwise 段階的に増加した。
-
SLE 患者が最も多く、ANA 陰性者が最も少なく、SLE 患者のみが I 型インターフェロンを多く発現していた Arthritis Rheumatol. 68, 2492–2502 (2016).
-
この発現パターンは、SLEの進行とセルフメンテナンスにおいてに、I型インターフェロンの役割と関連している Int. Immunopharmacol. 40, 542–549 (2016).
-
しかし、インターフェロンシグネチャーはdefined CTDを持たないANA陽性者のかなりの割合に見られる Arthritis Res. Ther. 19, 41 (2017).
-
このシグネチャーは、 臨床的なCTD の症状のぞんざいや進展ではなく、 ANA の力価や自己抗体の種類と関連しているようである ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT02234388 (2021).
-
-
結論としてインターフェロンシグネチャーは有望ではあるが、診断検査の付加価値を十分に解明するためにはさらなる研究が必要である
【Advancing nomenclature】
-
SLEの基礎となる免疫調節異常についての理解は進んでいるが、診断と分類は依然として難しい
-
疾患の一部の特徴のみを認める患者や他の自己免疫疾患とオーバーラップする特徴を有する患者を定義するための命名法は一貫していない
-
UCTDに加えて、occult, incomplete, incipient, possible, latent and probable SLEなどの用語が使用されている
-
SLEスペクトラム疾患の将来の定義は、疾患のサブグループを定義するための分子データがより増えて利用可能になるにつれて、現在の定義よりも高い特異性を持つようになるはずである
-
-
一方、共通の命名法を決定するために研究していくことは、臨床的な推論を組織化して、患者のサブセットを正確に特定するために重要である
-
UCTDの定義の改善に向けて、現在、いくつかの観察研究が進行中であり、この疾患を持つ患者の臨床症状や検査結果に関する情報を収集している Clinicaltrials.gov https://clinicaltrials.gov/ct2/show/NCT04402086 (2021).
-
このような研究の結果を分析することで、このタイプの自己免疫疾患患者の予後をより正確に予測することができ、また、SLEのようなより特異的なCTDへの進行の危険因子を特定することができるかもしれない
-
一方で臨床的な観点からは、症状や血清学的異常の発現から診断までの時間が、早期のSLEと安定したUCTDを遡及的に鑑別するための良い指標となるかもしれない
-
-
同様に、臨床研究に対する実用的な観点からincomplete SLEという言葉よりも具体的に‘early SLE’,という言葉を使用することも考えられるかもしれない
-
理由としては、分類可能なSLEではないが、SLEを強く示唆する特徴を持つ患者を同定するためである
-
例えば、ANAと抗DNA抗体陽性で、 malar rashがあるが、他にSLEの兆候や症状がない若い女性)など
-
-





